В работе исследована растворимость оксида Al в твердом растворе (CeO2)0,86(ZrO2)0,14 на примере исследования свойств системы (CeO2)0,75(ZrO2)0,125(Al2O3)0,125 методом функционала электронной плотности. Определены наиболее энергетически выгодные позиции дефектов в изучаемой системе. Определено влияние на технологически важные свойства – сделан вывод об образовании малоподвижных ассоциатов кислородных вакансий с Al с высокой энергией связывания Eass (1,08 эВ), снижающей конечную величину энергии активации ионной проводимости.
Ключевые слова: теория функционала электронной проводимости, компьютерное моделирование, CeO2, Al2O3.
Фазовые соотношения, физико-химические свойства композитов в системе CeO2-ZrO2-Al2O3 были подробно изучены в работах [1]. Материалы, обладающие высокой кислород-ионной проводимостью, имеют ряд технологических важных применений, таких как датчики кислорода и твердооксидные топливные элементы (ТОТЭ). Стандартным материалом ТОТЭ является оксид циркония, стабилизированный оксидом иттрия (YSZ). Однако ведется поиск материалов с более высоким коэффициентом диффузии по кислороду, и такими материалами являются твердые растворы на основе оксида Ce. Данные материалы обладают большей ионной проводимостью, чем YSZ и являются перспективными для создания низкотемпературных ТОТЭ. Для описания механизма ионной проводимости используются значения «энергии активации ионной проводимости», рассчитываемые по наклону температурной зависимости удельной электропроводности [2,3]. Материалы с низкой энергией активации ионной проводимости способны демонстрировать более высокую ионную проводимость при более низких температурах. Однако оксид Ce трудно спечь при температуре менее 1600°С, для чего используются различные спекающие добавки, например оксиды Co, Al и Ga [4,5]. При использовании данного метода спекания важно знать предел растворимости, поскольку добавки в количестве, не превышающем предел растворимости способны понизить температуру спекания. Авторы работы на примере системы (Ce0,8Gd0,2O1,9)1-x(Al2O3)x (x=0-0,05) определяли предел растворимости оксида Al [5]. Как выявлено, в твердом растворе на основе оксида Ce растворяется менее 10 мол. % Al2O3.
Вопросы о размещении иона Al в структуре твердого раствора с позиций точечных дефектов, о влиянии растворения Al2O3 на электрические свойства композитов в системе CeO2-ZrO2-Al2O3 недостаточно изучены [6]. Интересно было бы более подробно исследовать зависимости проводимости и ионной доли электропроводности композитов в данной системе от содержания оксида Al.
Согласно исследованиям методами рентгеновской дифракции композиционных порошков составов (ZrO2)0,87(СеО2)0,13 + 5 мол. % Al2O3 и (ZrO2)0,87(СеО2)0,13 + 10 мол. % Al2O3, присутствие фазы α-Al2O3 не наблюдается, что, скорее всего, связано с частичным растворением α-Al2O3 (1-2 мол. %) в твердом растворе (ZrO2)0,87(СеО2)0,13. Этому способствует наличие у Al3+ малого ионного радиуса (0,57 Å) по сравнению с радиусами ионов Zr4+ (0,82 Å), Се3+ (1,02 Å), и Ce4+ (0,88 Å). Такой эффект является очень важным, т. к. затормаживает рост зерна и увеличивает наноразмерность керамики [6-8].
Как видно из литературы, не проводились исследования влияния частичного растворения оксида Al на кислород-ионную проводимость, на одно из наиболее важных свойств твердых растворов на основе CeO2, определяющих эксплуатационные свойства таких изделий, как газовые сенсоры, катализаторы, топливные элементы.
Все расчеты периодических твердых тел методом функционала электронной плотности (англ. density functional theory, DFT) были выполнены с использованием программного пакета SIESTA [9,10]. Исходными данными в методе DFT служат заряды ядер и их положения в молекуле или кристалле и наборы базисных функций (как правило, слейтеровского или гауссового типов). SIESTA является как методом, так и его реализацией в виде компьютерной программы, для выполнения эффективных расчетов электронной структуры и расчетов методом ab initio молекулярной динамики молекул и твердых тел [11]. Для учета обменно-корреляционных эффектов использовалось приближение GGA (PBE) [12,13]. Для всех элементов базисный набор был расширен использованием двойной-ζ плюс поляризационная численных атомных орбиталей. Остовные электроны учитывались с помощью сохраняющего норму псевдопотенциала, построенного по схеме Труллера–Мартинса [14]. Для более точного вычисления полной энергии и связанных с ней величин энергия обрезания была поднята до 800 Ry. Поскольку для проведения исследования использовались достаточно большие 4x2x2 суперъячейки (до 47 атомов) и большая энергия обрезания, при вычислении полной энергии использовалась только одна k-точка в зоне Бриллюэна (а именно Γ-точка). Оптимизацию геометрии проводили методом сопряженных градиентов до тех пор, пока все силы, действующие на отрелаксированные атомы, не становились меньше 0,04 эВ/Å.
Анализируя смещения атомов (Рис. 1), следует отметить, что внутренние напряжения атомов, возникающие вследствие различия ионных радиусов ионов играют решающую роль – ионы кислорода ближе друг к другу в местах расположения допантов с меньшим чем у Ce ионным радиусом (Zr, Al) (Рис. 1, в,г).
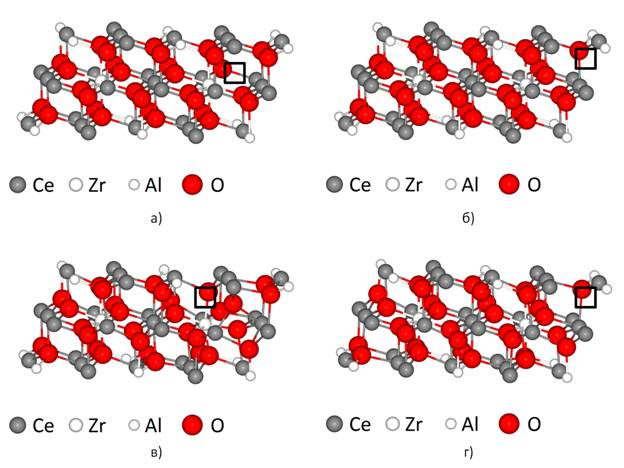
Рис. 1. Вид сбоку суперячеек, использовавшихся для исследования свойств системы (CeO2)0,75(ZrO2)0,125(Al2O3)0,125, где □ обозначает пустую вакантную анионную позицию. Первоначальный (до выполнения оптимизации геометрии) вид суперячеек с кислородной вакансией расположенной вблизи иона Zr (а) и вблизи иона Al (б). Соответствующий вид суперячеек после выполнения оптимизации геометрии (в,г). При сравнении рисунков (а) и (в) видно как в процессе оптимизации геометрии кислородная вакансия смещается из позиции вблизи иона Zr к позиции вблизи Al
В случае расположения кислородной вакансии вблизи Zr (Рис. 1,г, Рис. 2) необходимо отметить, что ионы кислорода смещаются сильнее, чем катионы, чему способствует способность материала к кислородно-ионной проводимости; их смещения носят хаотический характер, однако можно обнаружить, что ионы кислорода из целой области смещаются в сторону вакансии. Структурные искажения становятся настолько выраженными, что ион кислорода даже мигрирует на 1,43 Å в сторону вакансии, создавая вакансию вблизи Al, имеются даже смещения катионов (ион Al смещается на 0,27 Å). Следует отметить, что оптимизация геометрии проводилась до величины остаточной силы, превышающей 0,04 эВ/Å (0,08 эВ/Å), и была остановлена на 47-м шаге, поскольку, по всей видимости, данные мигрирующие ионы кислорода смещаются в новое положение на достаточно значительное расстояние. Такой расчет предъявляет высокие требования к вычислительным ресурсам, которые мы неспособны удовлетворить в данной работе. В первоначальном положении система находилась в существенно неравновесном состоянии и в процессе оптимизации геометрии происходило значительное уменьшение полной энергии – выигрыш в энергии (на суперячейку) вследствие релаксации ионов велик и составил 9,35 эВ.
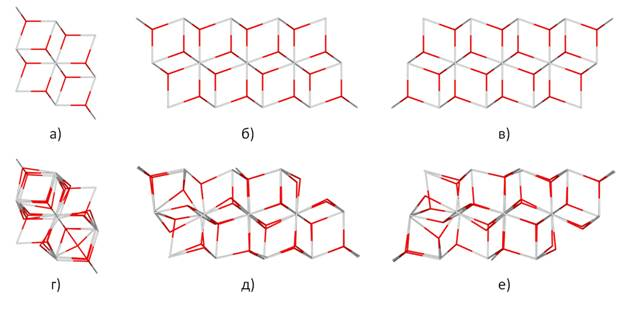
Рис. 2. Вид суперячейки, использовавшейся при компьютерном моделировании свойств твердого раствора (CeO2)0,75(ZrO2)0,125(Al2O3)0,125 с кислородной вакансией, расположенной вблизи иона Zr. Вид в трех проекциях до выполнения оптимизации геометрии (а,б,в), и после выполнения оптимизации геометрии (г,д,е). Изображение представлено в каркасном представлении, где светлые линии отражают положение катионов; красные, темные – положения анионов
В случае расположения кислородной вакансии вблизи Al (Рис. 1,в, Рис. 3) ионы кислорода смещаются более ограничено с отсутствием хаотического разупорядочения, катионы почти не смещаются из своих первоначальных позиций. Выигрыш в энергии вследствие релаксации структуры, несмотря на это также велик и составил 9,64 эВ (на суперячейку).
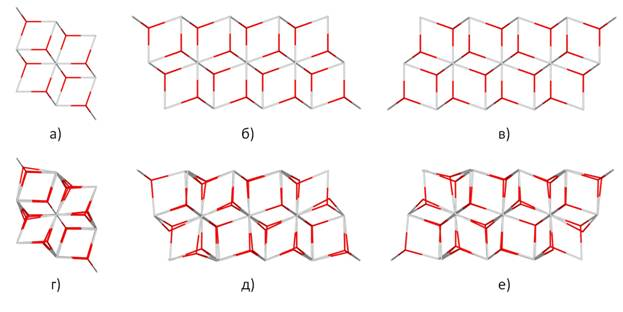
Рис. 3. Вид суперячейки, использовавшейся при компьютерном моделировании свойств твердого раствора (CeO2)0,75(ZrO2)0,125(Al2O3)0,125 с кислородной вакансией, расположенной вблизи иона Al. Вид в трех проекциях до выполнения оптимизации геометрии (а,б,в), и после выполнения оптимизации геометрии (г,д,е). Изображение представлено в каркасном представлении, где светлые линии отражают положение катионов; красные, темные – положения анионов
Интересно отметить, что в случае расположения кислородной вакансии вблизи Al имеются позиции ионов кислорода, которые после выполнения оптимизации геометрии почти не сместились из своих первоначальных позиций. Эффект влияния на ионы в кристалле оказывают взаимодействия двух типов: воздействие вследствие механических напряжений и электростатическое [2]. Равновесие всех сил, определяемых данными взаимодействиями, и действующих на данные ионы приводит к сохранению их первоначальных позиций после выполнения оптимизации геометрии.
Что касается поиска наиболее энергетически выгодных позиций дефектов в изучаемой системе, то расположение кислородной вакансии вблизи Al на 1,08 эВ энергетически более выгодно, чем вблизи Zr.
Кислород-ионная проводимость оксида церия невелика вследствие низкой концентрации вакансий кислорода. При этом энергия активации равна сумме энергии образования вакансии (Еf) и энергии миграции вакансии (Em). При легировании оксида Ce катионами с меньшей, чем у Ce валентностью в кристаллической решетке образуются кислородные вакансии. Данные вакансии электростатически взаимодействуют с введенными в кристаллическую решетку легирующими катионами с образованием малоподвижных ассоциатов (кластеров) с энергией связывания Eass, которые ограничивают подвижность кислородных вакансий. Таким образом, для легированного оксида Ce энергия активации может быть определена в данном случае как сумма Eass и Em [2]. Расчет любого из данных параметров важен для оценки величины энергии активации кислород-ионной проводимости, и сопоставление уже полученных величин (полных энергий ячеек с вакансиями, расположенными вблизи Al и Zr соответственно) позволяет оценить Eass. Таким образом, поскольку расположение кислородной вакансии вблизи Al на 1,08 эВ энергетически более выгодно, чем вблизи Zr, то величина Eass будет составлять 1,08 эВ. Данная величина энергии связывания ассоциатов Eass достаточно велика – так, для оксида Ce, легированного 13 мол. % оксида Gd суммарная энергия активации составляет 0,70 эВ [15]. Столь большая величина Eass повысит суммарную энергию активации ионной проводимости, затрудняя кисород-ионный транспорт. Таким образом, процесс растворения оксида Al является нежелательным и ухудшает технологически важные свойства материалов на основе оксида Ce.
Расчет энтальпии растворения ∆Hs оксида Al на одну формульную единицу Al2O3 производен нами с использованием значений полной энергии соответствующих фаз аналогично [3,6]. Для процесса растворения оксида Al в структуре твердого раствора можно записать:
Ce1-xZrxO2 + yAl2O3 → Ce1-xZrxAl2yO2-d, (1)
тогда
∆Hs = [E(Ce1-xZrxAl2yO2-d)-E(Ce1-xZrxO2)-E(yAl2O3)]/y. (2)
Полученные нами значения составляют -0,05 эВ и 1,03 эВ для кислородной вакансии расположенной вблизи Al и Zr соответственно. В связи с этим, процесс растворения может осуществляться при ∆Hs < 0 (для кислородной вакансии расположенной вблизи Al). Данный вывод согласуется с экспериментальными данными авторов [5], полученных для системы (Ce0,8Gd0,2O1,9)1-x(Al2O3)x (x=0-0,05).
Данные расчеты позволяют сделать предположение о том, что оксид Al может беспрепятственно растворяться в кристаллической структуре CeO2, легированном оксидом Zr при спекании, отжигах и термообработке, особенно по границам зерен. Даже незначительное растворение может оказать влияние на технически важные свойства – так, растворение Al2O3 в пределах 2 мол. % сопоставимо с легированием 4 мол. % РЗЭ твердых электролитов на основе CeO2, используемых для создания топливных элементов. Предварительные оценки влияния растворения оксида Al на энергию активации кислород-ионной проводимости позволяют сделать вывод об образовании малоподвижных ассоциатов кислородных вакансий с Al с высокой энергией связывания Eass, снижающей конечную величину энергии активации ионной проводимости. Таким образом, приводимые расчеты показывают, что процесс растворения оксида Al является нежелательным, ухудшающим важные свойства материалов на основе оксида Ce определяющие эксплуатационные свойства изделий на его основе, таких как газовые сенсоры, катализаторы, топливные элементы. Более подробное экспериментальное и теоретическое исследование влияния растворения оксида Al на технически важные свойства требуют дальнейших исследований.
Литература:
1. Tikhonov P.A., Arsent'ev M.Yu., Kalinina M.V., Popov V.P., Andreeva N.S., Podzorova L.I., Il'icheva A.A. Preparation and properties of ceramic composites with oxygen ionic conductivity in the ZrO2-CeO2-Al2O3 and ZrO2-Sc2O3-Al2O3 systems // Glass Physics and Chemistry, 2008, vol. 34, no. 3, pp. 319-323.
2. Andersson D.A., Simak S.I., Skorodumova N.V., Abrikosov I.A., Johansson B. Optimization of ionic conductivity in doped ceria // Proceedings of the National Academy of Sciences of the United States of America, 2006, vol. 103, no.10, pp. 3518-3521.
3. Арсентьев М.Ю., Тихонов П.А., Калинина М.В., Андреева Н.С. Исследование некоторых физико-химических свойств керамики, монокристаллов и наноразмерных пленок на основе оксидов циркония, гафния и РЗЭ // Физика и химия стекла, 2010, т. 36, № 4, С. 596-603.
4. Zhang T., Hing P., Huang H. and Kilner J. Sintering and grain growth of CoO-doped CeO2 ceramics // J. Europ. Ceram. Soc., 2002, vol. 22, iss. 1, pp. 27-34.
5. Lee J.S., Choi K.H., Ryu B.K., Shin B.C., Kim I.S. Solid Solubility Limits of Al2O3 and Ga2O3 in Gd2O3-Doped CeO2 // Journal of Materials Science Letters, 2003, vol. 22, iss. 24, pp. 1805-1807.
6. Arsent'ev M.Y., Tikhonov P.A., Kalinina M.V. Physicochemical properties of nanocrystalline composites based on ZrO2, Al2O3, and rare-earth oxides // Glass Physics and Chemistry, 2011, Т. 37, № 4, С. 450-458.
7. Панова Т.И., Арсентьев М.Ю., Морозова Л.В., Дроздова И.А. Синтез и исследование нанокристаллической керамики в системе ZrO2-CеO2-Al2O3 // Физика и химия стекла, 2010, т. 36, № 4, С. 470-477.
8. Panova T.I., Arsent'ev M.Yu., Morozova L.V., Drozdova I.A. Synthesis and investigation of the structure of ceramic nanopowders in the ZrO2-CeO2-Al2O3 system // Glass Physics and Chemistry, 2010, vol. 36, no. 4, pp. 470-477.
9. Soler J.M., Artacho E., Gale J.D., Garcia A., Junquera J., Ordejon P., Sanchez-Portal D. The SIESTA method for ab initio order-N materials simulation // J. Phys. Condens. Matter, 2002, vol. 14, no. 11, pp. 2745-2779.
10. Junquera J., Paz O., Sanchez-Portal D., Artacho E. Numerical atomic orbitals for linear-scaling calculations // Phys. Rev. B, 2001, vol. 64, iss. 23, pp. 235111(9 pages).
11. http://departments.icmab.es/leem/siesta/
12. Perdew J.P., Burke S., Ernzerhof M. Generalized Gradient Approximation Made Simple // Phys. Rev. Lett., 1996, vol. 77, iss. 18, pp. 3865-3868.
13. Hammer B., Hansen L.B., Norskov J.K. Improved adsorption energetics within density-functional theory using revised Perdew-Burke-Ernzerhof functionals // Phys. Rev. B, 1999, vol. 59, iss. 11, pp. 7413-7421.
14. Troullier N., Martins J.L. Efficient pseudopotentials for plane-wave calculations // Phys. Rev. B, 1991, vol. 43, iss. 3, pp. 1993-2006.
15. Ivanov V., Khrustov V., Kotov Y., Medvedev A., Murzakaev A., Shkerin S., Nikonov A. Conductivity and structure features of Ce1−xGdxO2−δ solid electrolytes fabricated by compaction and sintering of weakly agglomerated nanopowders // J. Eur. Ceram. Soc., 2007, vol. 27, iss. 2-3, pp. 1041-1046.







