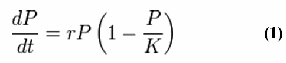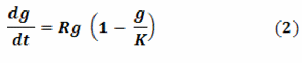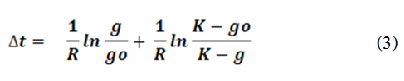В настоящей работе был сформулирован комплекс представлений о неоднородности процессов старения высших эукариот на клеточном уровне. Подобная гетерогенность выражается, прежде всего, в переходе организма, на клеточном уровне, в процессе онтогенеза, от старения летального типа, превалирующего на ранних этапах индивидуального развития, к старению витального типа, которое свойственно уже более поздним стадиям постнатального развития. Получены данные, свидетельствующие о присутствии обратной зависимости между возрастной динамикой экспрессии целого ряда митогенов и изменением продолжительности пресинтетического периода жизненного цикла эукариотических клеток. Приведенные данные свидетельствуют в пользу того, что основой позиционируемой неоднородности процессов старения является R/K – инверсия или перемена жизненной стратегии развития организма на молекулярно-клеточном уровне.
Ключевые слова: летальный тип старения, витальный тип старения, продолжительность G1-фазы, митогены, правило Хейфлика, R/K-инверсия.
Современный взгляд на проблему биологического старения
Старение как явление наблюдается практически у всех организмов. В самом общем смысле биологическое старение можно определить как изменение биологических особенностей организма, возникающее с наступлением зрелости и выражающееся в постепенном снижении адаптационных свойств организма. Подобные изменения могут затрагивать как функцию отдельных клеток, так и целый организм, т.е. старение представляет собой совокупность возрастзависимых отклонений от гомеостаза на молекулярном, субклеточном, клеточно-тканевом и системном уровнях [1]. Фундаментальная наука выделяет генетические теории старения, когда запрограммированные на генетическом уровне «биологические часы» регулируют процессы онтогенеза, нейроэндокринные теории, а также теории накопления повреждений. Однако это разделение довольно условно. В настоящее время превалируют две большие группы теорий старения: стохастические (вероятностные) теории и теории программированного старения [2].
Общая характеристика динамических моделей в биологии популяций
Важным параметром, характеризующим реальные сообщества является ограниченность ресурсов или емкость экологической ниши (К) – это максимально возможная численность популяции в данных условиях. Для популяций характерен также прирост, биотический потенциал или мальтузианский параметр (r). Прирост популяции может быть положительным, нулевым и отрицательным. При увеличении численности популяции эта величина линейно уменьшается. В этом случае темп роста популяции описывается логистическим уравнением Ферхюльста (1) [3]:
где P - численность популяции, t - время, параметр r характеризует скорость роста (размножения), а K— ёмкость среды.
Исходя из названия коэффициентов, в экологии часто различают две стратегии поведения видов: r-стратегия предполагает бурное размножение и короткую продолжительность жизни особей и К-стратегия — низкий темп размножения и долгую жизнь особей в популяции. Популяции видов, у которых рождаемость и смертность в значительной мере зависят от действия внешних факторов, подвержены быстрому изменению биотического потенциала. Эти популяции редко достигают численности К и существуют за счет высокой плодовитости (высокое значение rmax). Такой способ сохранения популяций называется R–стратегия. R–Стратеги характеризуются высокой плодовитостью, низкой конкурентоспособностью, быстрым развитием и короткой продолжительностью жизни. Популяции видов, у которых рождаемость и смертность в значительной мере зависят от их плотности, в меньшей степени зависят от действия внешних факторов. Эти популяции называются равновесными, или стационарными. Они поддерживают численность, близкую к величине К, поэтому способ сохранения таких популяций называется К–стратегия. К–Стратеги характеризуются более низкой смертностью, высокой конкурентоспособностью, длительным развитием и длительной продолжительностью жизни. Имеющиеся биогенные показатели, такие как продолжительность отдельных стадий жизненного цикла и уровень экспрессии некоторых внутриклеточных митогенов, указывают на то, что клетки, составляющие клеточные популяции макроорганизма, последовательно проходят в своём развитии этапы R- и K- стратегии.
Стареющая клетка как структурно-функциональная единица стареющего организма
Клеточный цикл это повторяющаяся, с определённой регулярностью, совокупность событий, обеспечивающих деление клеток. Клеточный цикл любой клетки включает несколько неизменных стадий: G1 – фаза - период перед синтезом ДНК или пресинтетический период, S-фаза - период синтеза или репликации ДНК, G2-фаза - период между синтезом ДНК и митозом, а также завершающий этап - собственно, митоз [4]. Неизменные по очерёдности, эти фазы, однако, могут иметь разную продолжительность, что зависит от ряда факторов, важнейшими из которых, предположительно, являются возраст организма и тип клеток. В 1961 г. профессор стенфордского университета Леонард Хейфлик, при проведении серии уникальных опытов, получил результат, свидетельствующий о способности эукариотических клеток, даже в идеальных условиях культивирования, делиться только ограниченное число раз (50±10) [5]. Было установлено также, что при пересевах клетки проходят in vitro ряд морфологически различимых стадий, после чего их способность к пролиферации постепенно утрачивается. Последняя фаза жизни клеток в культуре была приравнена к клеточному старению, а сам феномен получил, по имени автора, название предела Хейфлика. Первым следствием из этого правила является факт того, что с увеличением возраста донора клеток, число делений, на которые способны клетки организма, существенно уменьшается, что приводит к представлению о существовании некоего «счетчика» делений, ограничивающего общее их число, при этом целесообразно отметить, что переход клетки из одной её жизненной фазы в другую определяется особыми белками-митогенами называющимися циклинами, а также их ко-регуляторами, такими как, например, ядерные рецепторы к стероидным гормонам вкупе с их гормональными лигандами [6]. После экспрессии, под влиянием стимулирующих факторов циклины взаимодействуют с циклинзависимыми киназами, образуя активный холоэнзим, который призван фосфорилировать белки-мишени, участвующие в инициации процессов, приводящих к смене фаз клеточного цикла [7, 8]. Из множества циклинов, наиболее интересным, прежде всего с точки зрения настоящей работы, является циклин D1, определяющий этап перехода клетки из фазы G1 к S-фазе, т.е. к подготовительному этапу перед клеточным делением. Таким образом, на основании всего сказанного выше, можно сформулировать основную цель данной работы как изучение зависимости продолжительности G1 периода интерфазы клеточного цикла от возраста донора клеточного материала, на примере пульпарных фибробластов, а также изучение взаимосвязи данных процессов с возрастными изменениями уровней экспрессии циклина D1 и ядерных рецепторов (на примере рецепторов к андрогенам - AR).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Получение клеточных линий фибробластов человека
Источником фибробластов служила зубная пульпа, полученная из удалённых зубов людей мужского пола разного возраста [9]. Доноры клеток были сгруппированы в соответствии с возрастом на следующие группы: 15-20, 25-40, и 55-75 лет. Ткани, извлечённые из пульпы предварительно очищенного и раздробленного зуба в стерильных условиях измельчались и переносились в среду M199 с 1% фетальной сывороткой (FCS), соответствующими антибиотиками и 1 мг/мл бычьего сывороточного альбумина. Ткани пульпы обрабатывались коллагеназой и ДНКазой в течение одного часа при 36оС. Действие ферментов прерывалось посредством добавления охлаждённой среды Игла МЕМ с солями Эрла, с глутамином (ПанЭко, Россия) в 1% FCS с соответствующими антибиотиками. После отмывки, суспензия пульпарных клеток центрифугировалась в течение 5 мин. при 4000 об/мин, после чего осадок ресуспендировался в том же объёме среды Игла МЕМ с 5% FCS, переносился в стерильные плашки и инкубировался при 37оС в атмосфере 5% CO2 для миграции клеток из эксплантатов [10]. После достижения первичной культурой состояния монослоя, она обрабатывалась трипсином (0,02%) в течение 10-15 мин, после чего трипсин удалялся, и клетки вновь суспендировались в той же среде. Затем проводился рассев в новые флаконы, в итоге получали клеточную культуру, готовую для дальнейшего субкультивирования. Субкультивирование производилось до достижения клетками 70% от монослоя в среде Эрла с глутамином и добавлением 10 % фетальной сыворотки, помимо этого, для имитации естественного гормонального фона организма, в качестве основного лиганда андрогеновых рецепторов, в среду добавлялись 0,1- 0,2 мкМ тестостерона.
Проведение полимеразной цепной реакции (ПЦР), сопряженной с обратной транскрипцией.
Изучение экспрессии целевых митогенов проводилось косвенно, на основании данных об уровне экспрессии их мРНК. Суммарную РНК выделяли с использованием реактива «TRIZOL» (Life Technologies, Inc.) согласно рекомендациям производителя, базирующимся на стандартной методике [11]. Синтезированная кДНК использовалась для амплификации методом ПЦР со специфическими праймерами. Для амплификации гена циклинаD1 были спланированы праймеры For-СD1-5’– ATGGAGCACCAGCTGCTGTGCTGCGA - 3’; Rev-CD1 5’-GATGTCCACGTCCCGCACGTCGGTG - 3’; для амплификации гена AR были спланированы праймеры, комплементарные к наиболее константным областям обеих изоформ АR: ForAR–5’–AACGACTGCACCATCGACAAGTTCC-3’; RevAR - 5’ –GCACGGAGATGATCTCGGCCATCATCT- 3’. Режим амплификации точный: 95оС – 3 мин; (94оС – 10с, 60 оС - 30с, 72оС – 2 мин)x25 (кол-во циклов); 10оС – хранение.
Количественно-конкурентный метод ПЦР
Метод основан на совместной амплификации матрицы целевой ДНК (амплификанты генов циклинов и андрогеновых рецепторов) и определённого количества внутреннего ДНК-стандарта (конкурента), несущего те же сайты связывания для праймеров [12, 13]. Так, как исходное содержание конкурента известно, и принимая, что эффективность амплификации целевого гена и конкурентной ДНК одинакова, соотношение количества двух продуктов ПЦР, определяемое электрофоретически при помощи компьютерной программы DNA Gel Analysis Software (Helicon), представляет собой соотношение целевой ДНК и ДНК конкурента в пробе до амплификации. Конкурентом является синтетическая последовательность целевых генов с запланированной центральной делецией для того, чтобы в ходе ко-амплификации получить фрагменты, отличающиеся по молекулярному весу на электрофореграмме.
Статистическая обработка результатов исследования.
Культуры клеток пульпарных фибробластов получались от репрезентативной выборки представителей разных возрастных групп (мужчины в возрасте 15 - 20 лет, 25 - 40 лет, 55-75 лет) по принципу, описанному в материалах и методах. Клетки культивировались в повторах, для последующего изучения экспрессии генов с периодичностью каждые два часа. Статистическая обработка результатов исследований проводилась при помощи программы Statistic 5.773, методом вариационной статистики, включая вычисление средних величин (М) и стандартных ошибок средних величин (±m). Для оценки достоверности различий средних величин применяли критерий Стьюдента td [14]. Достоверной считали значимость p≤0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В процессе анализа литературных данных была выдвинута гипотеза, заключающаяся в том, что одним из основных условий увеличения продолжительности жизненного цикла клеток эукариот по мере взросления макроорганизма, является увеличение пресинтетического периода их интерфазы. Известно, что основными физиологическими факторами, определяющими и ускоряющими процесс перехода клетки из фазы G1 в фазу S являются митогены белковой природы, к основным из которых можно отнести циклин D1 [15], экспрессирующийся в первой половине G1 фазы под влиянием ядерных рецепторов и их гормональных лигандов. При этом концентрация циклина, обычно, достигает своего максимума к середине G1 периода и снижается до минимума к началу S периода. Таким образом, циклин D1 вполне мог рассматриваться в качестве некоего маркера смены периодов жизненного цикла клеток. Производилось выделение тотальной клеточной РНК для проведения ОТ-ПЦР и количественно-конкуррентной ПЦР. Определение количества ПЦР продукта проводилось при помощи программы DNA Gel Analysis Software (Helicon).
В процессе работы было сделано предположение, что внутриклеточная концентрация данных митогенов и их ко-регуляторов не стабильна не только в течение жизненного цикла клетки, но и на протяжении жизни организма в целом. Для проверки данной гипотезы были получены культуры клеток фибробластов от репрезентативной выборки мужчин разных возрастных групп по принципу, описанному в материалах и методах. Так как науке известны факты стимулирующего влияния ядерных рецепторов на биосинтез циклинов [16], то в полученных клетках также определялся и уровень экспрессии мРНК рецепторов к андрогенам, для ориентировочной оценки корреляции их количественного изменения с динамикой возрастных изменений уровня экспрессии циклина D1 и продолжительности G1- периода. Для повышения точности определения в пробы вводили ДНК-конкурент, представлявший собой синтетические гены циклина и рецепторов к андрогенам, с индуцированной центральной делецией для последующего различения амплификантов гель-электрофоретически (синтез делетированных генов производился в ЗАО Евроген, Россия). Соотношение количества ПЦР-продукта и его конкурента эквивалентно соотношению целевой ДНК и конкурента в пробе до амплификации. При этом за 100% уровень экспрессии изучаемых митогенов принималась наибольшая их концентрация у молодых доноров в начальный период культивирования клеток (рис.1.a.).
Определение референсных пределов уровней экспрессии мРНК циклина D1 в клетках, полученных от доноров разного возраста, позволило оценить его динамику на протяжении интерфазы, при этом, благодаря цикличности экспрессии митогена, пресинтетический и синтетический периоды были хорошо дифференцируемы.
Рис. 1. - a.) – Динамика экспрессии мРНК циклинаD1 и рецепторов к андрогенам пульпарных фибробластов, полученных от доноров разных возрастных групп (за 100% уровень экспрессии белка принимается максимум экспрессии соответствующего белка у молодых особей). b.) – Общий вид зависимости продолжительности G1- периода интерфазы от возраста донора клеточного материала.
Результаты данных исследований свидетельствовали в пользу предположения о возрастопосредованной обратной зависимости между динамикой экспрессии циклина D1 и рецепторов к андрогенам и продолжительностью G1-периода клеточного цикла эукариот (рис 1.a.,b.). Настоящее исследование показывает также, на примере АR, что в разные возрастные периоды одинаковый гормональный фон оказывает различное влияние на длительность интерфазы однотипных клеток, что обусловлено прежде всего разным уровнем экспрессии соответствующих рецепторов и разной степенью чувствительности клеток одного и того же типа к гормональным лигандам.
R/K – инверсия клеток эукариот как основа онтогенетического перехода организма от летального типа старения к витальному
Анализ литературы и полученные теоретические и научно-практические данные, касающиеся зависимости продолжительности интерфазы от уровня экспрессии митогенов, свидетельствуют, что в процессе индивидуального развития клетки многоклеточного организма в соответствующих клеточных популяциях, в определённый момент времени, в целях «самосохранения», вступают на путь перемены собственной жизненной стратегии, что выражается в увеличении времени между последующими митотическими делениями, по мере взросления организма, за счёт постепенного роста продолжительности G1 периода интерфазы клеток (рис.1.b.), чему сопутствует и, вероятно, способствует возрастное снижение уровня экспрессии таких митогенов и корегуляторов как циклин D1 и ядерные рецепторы (рис.1.a.). В настоящей статье эти данные являются опорной точкой для формирования представлений о том, что законы описывающие динамику популяций организмов, могут быть применены и для описания динамики развития популяций клеток в процессе онтогенеза отдельно взятого организма. Мы полагаем, что в процессе индивидуального развития, клетки высших эукариот претерпевают постепенную молекулярно-генетическую инверсию своих жизненных принципов, что выражается в смене так называемой «R» - стратегии существования на «К» - стратегию. Для большей ясности тут необходимо отметить, что под «R» - стратегией, применительно к клеткам, мы понимаем стратегию расточительства, характерную для ранних этапов онтогенеза индивидуума, заключающуюся в коротком жизненном цикле клеток, преимущественно за счёт сокращённого G1 - периода их интерфазы, что проявляется в интенсивном обновлении клеточных поколений. Подобная стратегия превалирует у молодых форм, обеспечивая собственно фенотипическое проявление молодости как таковой, выражающееся в слаженности работы всех органов и систем и в высокой регенеративной способности тканей. Однако длительное поддержание стратегии «молодости» чрезвычайно не выгодно клеткам любого живого существа, так как оно требует постоянной высокой метаболической напряженности, которая истощает как отдельные клетки, так и организм в целом, подталкивая его на путь скорого (летального) старения. В качестве примера данных слов можно привести негативное влияние «R»-клеточной стратегии на продолжительность жизни миграционных рыб семейства лососевых (Salmonidae) [17]. И именно для противодействия подобным негативным моментам, по нашему мнению, в клетках многих высокоорганизованных эукариот, эволюционно, на генотипическом и, вероятно, также на эпигенетическом уровне, начал вырабатываться единый механизм «демпфинга» прогрессии клеточного цикла, позволяющий подавляющему большинству клеток, на определённом этапе постэмбрионального развития, перестраиваться с расточительной «R» - стратегии существования на умеренную «К» - стратегию. В чём же, спрашивается, преимущество «К» - стратегии над «R» - клеточной стратегией? Преимущество сводится к снижению скорости размножения и увеличению степени выживаемости клеток в режиме щадящего (витального) старения, которое обеспечивается снижением напряженности обменных процессов и увеличении продолжительности интерфазы клеточного цикла, преимущественно за счёт уменьшения уровня экспрессии митогенов и корегуляторов, что, в итоге, приводит к редукции частоты смены клеточных поколений (следует отметить, что частота смены клеточных поколений в разных тканях имеет свои особенности, однако мы говорим о тенденции, которая имеет общую направленность для всех клеток организма). «К» - стратегия превалирует у возрастных организмов, обеспечивая, собственно, фенотипические проявления старости, выражающиеся в падении слаженности работы органов и систем, снижении регенеративной способности тканей, прежде всего ввиду «физиологической усталости» клеток с увеличенной интерфазой. Кроме того ярким фенотипическим проявлением активации подобной стратегии является общеизвестное накопление в клетках избыточного количества различного рода включений (меланин, липофусцин и др.), вовлечённых в противодействие окислительному стрессу. Аналогия с динамикой популяций макроорганизмов позволяет, для описания динамики жизненного цикла клеточных популяций, применить модифицированное логистическое уравнение, разработанное бельгийским математиком Ферхюльстом (2) [3]:
Как видно, уравнение (2) представляет собой дифференциальное уравнение первого рода с разделяющимися переменными. Произведя ряд соответствующих преобразований выражения (2) можно найти интервал времени ∆t, за который клетки-представители однородной ткани многоклеточного организма достигнут предельных значений G1-периода в ходе онтогенеза (3):
R
–
коэффициент, отражающий скорость, с которой фаза G1
достигает своих максимальных значений;
![]() – продолжительность G1-периода
интерфазы на начальных этапах онтогенеза;
– продолжительность G1-периода
интерфазы на начальных этапах онтогенеза;
![]() - продолжительность
пресинтетического периода на конечных этапах онтогенеза; ∆t
–
интервал времени; К
– асимптотическое
значение g
(то есть, видовой физиологический предел величины пресинтетического
периода).
- продолжительность
пресинтетического периода на конечных этапах онтогенеза; ∆t
–
интервал времени; К
– асимптотическое
значение g
(то есть, видовой физиологический предел величины пресинтетического
периода).
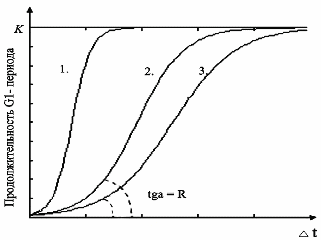
Рис.2. – Семейство идеализированных S-образных кривых, характеризующих динамику жизненного цикла клеток в составе организма (Δt–интервал времени (из формулы-3), за который большинство морфологически однородных клеток организма увеличивают свой G1-период до максимальных значений; график 1 характерен для клеток с R-стратегией, в то время как кривая 3 типична для клеток с К-стратегией).
Решением уравнения (3) является график, который в идеализированном виде представляет собой стандартную S-образную кривую, угол наклона которой определяется величиной коэффициента «R» (4) (рис.2.).
Физиологический смысл уравнения (3) сводится к тому, что по мере роста параметра «R», т.е. скорости достижения фазой G1 своих максимальных значений, морфологически однородные клетки организма быстрее приближаются к пределу Хейфлика. Таким образом, высокие значения коэффициента «R» являются условиями, определяющими «R» - стратегию существования клеток эукариот (рис.2.).
ЗАКЛЮЧЕНИЕ И ВЫВОДЫ
Полученные теоретические и научно-практические результаты свидетельствуют о том, что с увеличением возраста донора клеток увеличивается время между последующими клеточными делениями, за счёт более продолжительного пребывания клеток в G1 периоде интерфазы, вследствие возрастного снижения уровня экспрессии митогенов, приводящего, фактически, к возрастному повышению порога чувствительности клеток-мишеней к регулирующим сигналам. Иными словами, идентичные по своему тканевому происхождению клетки старых и молодых организмов одного и того же вида, имеют различную продолжительность жизненного цикла, преимущественно за счёт разного времени их пребывания в пресинтетическом периоде интерфазы. Нами были введены понятия летального и витального типов старения, в соответствие с чем эукариоты могут быть разделены на две большие группы: жизненные формы с превалирующим летальным (скоротечным) типом старения, например многие насекомые и проходные рыбы, а также существа с витальным (медленным) типом старения, такие, например, как некоторые пресмыкающиеся и человек. В данной работе была сформулирована концепция R/K инверсионного сопротивления клеток эукариот старению летального типа. В соответствии с этой концепцией, у организмов с летальным старением преобладает расточительная стратегия R-типа с быстрой сменой поколений клеток и быстрым исчерпанием жизненного потенциала, в то время как клетки эукариот с витальным типом старения осуществляют в процессе онтогенеза обязательный инверсионный переход от R-жизненной стратегии к К-стратегии, проявляющейся возрастзависимым снижением уровня экспрессии внутриклеточных митогенов, медленной сменой клеточных поколений и сбережением жизненных ресурсов.
Литература:
Москалёв А. А.// Успехи геронтол. 2010. Т. 23. № 1. С. 9–20.
Schulz-Aellen M.-F. Aging and human longevity. Boston: Birkhauser, 1997. 283 p.
Базыкин А.Д. Нелинейная динамика взаимодействующих популяций. ИКИ, 2003.
De Souza C.C. and Osmani S.A. // Eukaryotic Cell. 2007. 6 (9):1521–1527.
Hayflick L. // Experimental Cell Research. 1965. V.37. P. 614–636.
Klein E. A., Assoian R.K. // Journal of Cell Science. 2008. V.121. C. 3853-3857.
Musgrove E.A., Lee C.L., Buckley M. F., Sutherland R.L. // Cell Biology. 1994. V. 91. P. 8022-8026.
Shankung Lin, Huey-Chung Huang // Mol Pharmacol. 2001. V.60. P. 768–775.
Tran-Hung L., About I. // European Cells and Materials. 2007. V.13. P.4.
Kasinathan P., Knott J.G., Moreira P.N. // Biology of Reproduction. 2001. V.64. P. 1487–1493.
Chomczynski P. & Sacchi N. // Nature Prot., 2006. V.1. P. 581–585.
Studer. E. // Z. Lebensm. Unters. Forsch. 1998. V. 207. P. 207-213.
- Hardegger. M. // Eur. Food Res Technol. 1999. V. 209. P. 83-87.
Куликов Л.В., Никишов А.А., Математическое обеспечение эксперимента. M.: - Издат. РУДН, 1994.
Resnitzky D., Reed S.I., // Mol. Cell. Biol. 1995. 15 (7): 3463–3469.
Dongho Geum, Woong Sun. //Mol. Reproduction and Development. 1997. V.46. P.450–458.
Maldonado T.A., Jones R.E., Norris D.O. // J. Neurobiol. 2002. V.53. P.21-35.