Изучено влияние мольного отношения SiO2/Al2O3 в цеолите на селективность образования ароматических углеводородов при превращении метанола. Показано, что увеличение мольного отношения SiO2/Al2O3 в цеолите приводит к снижению выхода ароматических углеводородов. Селективность по ароматическим углеводородам сильно зависит от изменения температуры и времени контакта. Показано, что п-ксилол является исходным веществом при формировании других ароматических углеводородов.
В ряде литературных источников [1,2] стабильность ВК-цеолитов типа ZSM по отношению к коксообразованию связывают со стерическими факторами. При этом небольшой объём каналов препятствует проникновению углеродистых отложений в объём цеолита. Однако это предположение находится в противоречии с результатами работ [3,4], свидетельствующих о том, что потеря активности цеолитов ZSM является результатом их отравления за счёт коксообразования.
Увеличение стабильности цеолитного катализатора и селективности реакции также может происходить при установлении определённого мольного отношения SiO2/Al2O3 и времени контакта на превращение метанола в ароматические углеводороды на цеолите типа ультрасила.
Экспериментальная часть
Модифицирование цеолитов проводили методом пропитки растворами гидрофосфата аммония, нитратов цинка и РЗЭ (La, Ho), с последующим высушиванием и прокаливанием при 3500С и 5500С по 4 часа, соответственно. Эксперименты проводили на установке проточного типа со стационарным слоем катализатора объёмом 4 см3 в реакторе идеального вытеснения при атмосферном давлении в присутствии водорода.
Анализ продуктов реакции осуществляли хроматографическим методом [5,6]. Кислотные свойства катализаторов определяли методом термопрограммированной адсорбции аммиака [6].
Влияние мольного отношения SiO2/Al2O3 в цеолите при постоянной объёмной скорости, температуры и давления (t=4200C, P=1,0 атм, v=1ч-1) на состав жидких углеводородов при превращении метанола представлено в таблице.
Таблица
Влияние мольного отношения SiO2/Al2O3 в цеолите на выход жидких углеводородов.
Условия: t=4200C, P=1,0 атм, v=1 час-1
|
№ |
Мольное отношение SiO2/Al2O3 |
Состав жидких продуктов, мас.% |
|
|
алифатических |
ароматических |
||
|
1. |
24 |
32,5 |
67,5 |
|
2. |
61 |
48,3 |
51,7 |
|
3. |
150 |
58,8 |
41,2 |
|
4. |
200 |
64,5 |
35,5 |
Видно, что увеличение мольного отношения SiO2/Al2O3 цеолитах от 24 до 200, приводит к увеличению содержания алифатических углеводородов от 32,5 мас.% до 64 мас.% и уменьшению доли ароматических углеводородов с 67,5мас.% до 35,5 мас.%.
Фракция жидких углеводородов, полученная в течение первых 2ч на цеолитах с мольным отношением SiO2/Al2O3=24, содержит 67,5 мас.% ароматических углеводородов и 32,5мас.% алифатических углеводородов С5-С7.
Совершенно иное соотношение ароматических и алифатических углеводородов получается на ультрасиле с мольным отношением SiO2/Al2O3 равным 200. Жидкая фракция, полученная на этом цеолите, содержит 35,5 мас.% ароматических углеводородов.
Следовательно, с увеличением мольного отношения SiO2/Al2O3 в цеолитах соответственно уменьшается выход ароматических углеводородов.
Выход жидких углеводородов также зависит от мольного отношения SiO2/Al2O3 в цеолите, температуры, времени контакта и работы катализатора.
На образцах с мольным отношением SiO2/Al2O3 равным 24-100 повышение температуры реакции с 300 до 4200С приводит к возрастанию выхода жидких углеводородов (с 7,1 до 16,5 мас.%). Дальнейшее повышение температуры приводит к уменьшению жидких продуктов. На образцах с мольным отношением SiO2/Al2O3 равным 120-200 максимальный выход жидких углеводородов (17,1 мас.%) достигается при 4500С.
Изучение влияния мольного отношения SiO2/Al2O3 в цеолите на стабильность работы показало, что с ростом мольного отношения наблюдается увеличение продолжительности работы катализатора. Например, если при времени контакта (τ) равном 0,5ч и температуре 4250С время стабильной работы Н-ультрасила с мольным отношением SiO2/Al2O3 равном 61 составляет 6ч, то на ультрасиле с мольным отношением SiO2/Al2O3 равном 200, время стабильной работы возрастает до 14ч. Увеличение стабильности работы ультрасила, очевидно, связано с уменьшением силы и концентрации кислотных центров при возрастании мольного отношения SiO2/Al2O3 в цеолите. Например, при увеличении мольного отношения SiO2/Al2O3 с 61 до 200 наблюдается значительное снижение концентрации сильных кислотных центров (с 528 до 321 мкмоль&#;г-1), которые ответственны за протекание процессов, приводящих к образованию кокса, блокирующего активные центры катализатора [7,9].
В процессе работы катализатора Н-ультрасила меняется распределение продуктов реакции как в газовой, так и в жидких частях катализата.
|
|
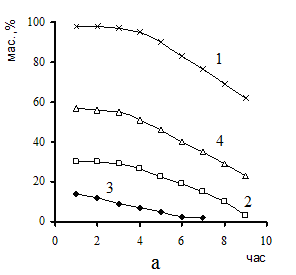
Рис.1 Зависимость распределения продуктов конверсии метанола от времени
работы ультрасила (а,б) при 4250С и τ=0,5ч:
1-общая конверсия метанола; 2-выход газообразных продуктов углеводородов С1-С4;
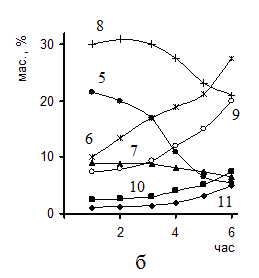
3 – выход жидких углеводородов С5-С10; 4 – Н2О; 5 – толуол; 6 –п-ксилол;
7 – о-ксилол; 8 – м-ксилол; 9- псевдокумол; 10 – метилэтилбензол; 11 – дурол.
На рис. 1а представлена характерная картина распределения продуктов реакции по мере отравления катализатора Н-ультрасила в процессе работы при 4250С и времени контакта τ=0,5ч. При этих условиях цеолит Н-ультрасил работает стабильно в течение 6 часов. Наблюдаемое в процессе работы Н-ультрасила постоянное нарастания выхода диметилового эфира и одновременное уменьшение выхода газообразных углеводородов ещё раз подтверждает высказанное ранее [10] предположение, что коксовыми отложениями отравляются только центры, активные в реакциях вторичных превращений углеводородов, а, следовательно, образование диметилового эфира и углеводородов идёт на разных центрах поверхности цеолитов.
Для газообразных углеводородов отмечены следующие закономерности:
содержание С1-С4 парафинов в катализате в течение времени непрерывно падает, а олефинов С2-С4 – проходит через максимум, положение которого с увеличением времени контакта и уменьшением температуры реакции смещается в сторону больших времен работы катализатора.
жидкая углеводородная фракция конверсии метанола в основном состоит из ароматических углеводородов, содержание которых составляет до 75% в зависимости от времени контакта и температуры, а максимальный выход жидких углеводородов при 100%-ной конверсии метанола, колеблется от 13,5 до 17,1 мас.%.
На рис.1 (б) представлено распределение ароматических соединений в жидком катализате в зависимости от времени работы Н-ультрасила при 4250С и τ=0,5ч. На рис. 1(б) представлены зависимость распределения основных компонентов жидкого катализата от времени контакта.
При 4200С и τ=0,5ч распределение ароматических углеводородов в жидком катализате в зависимости от времени работы ультрасила с мольным отношением SiO2/Al2O3 равном 61 следующее: в процессе работы катализатора содержание в катализате псевдокумола, метилэтилбензола и дурола увеличивается, а толуола м- и о-ксилолов уменьшается, содержание п-ксилола в отличие от этих изомеров растёт. С изменением температуры и времени контакта меняется отдельное содержание компонентов в смеси, а качественная картина распределения продуктов в катализате по мере дезактивации катализатора остаётся неизменной. С уменьшением времени контакта и температуры, содержание п-ксилола в катализате возрастает.
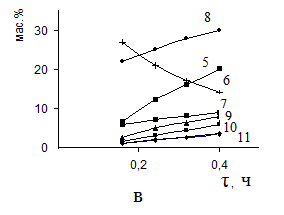
При всех изученных условиях отношение п-ксилола/о-ксилол либо превышает равновесное значение, либо стремится к нему при больших временах контакта и высоких температурах. Это свидетельствует о том, что практически при всех изученных условиях наблюдается предпочтительное образование п-ксилола по сравнению с его изомерами. Среди изомерных метилэтилбензолов преобладает п-этилтолуол, триметилбензол-псевдокумол и тетраметилбензол – дурол. Преимущественное образование п-ксилола и дурола по сравнению с их изомерами на ультрасиле можно объяснить особенностями структуры этого цеолита, обладающего селективностью специфичной к форме молекул. При температурах ниже 3500С и малых временах контакта фракция ксилолов на 95% состояла из п-изомера (рис.1в).
Такой характер зависимости изменения содержания п-ксилола со временем контакта позволяет утверждать, что п-ксилол может явиться исходным веществом при формировании других ароматических углеводородов.
В пользу этого утверждения говорят отмеченные выше экспериментальные факты предпочтительного образования п-ксилола, превышение отношения п-ксилол/о-ксилол и п-ксилол/м-ксилол над равновесными значениями, а также увеличение выхода п-ксилола с понижением температуры при одновременном уменьшении ароматических углеводородов.
- Литература:
Detertoq W.I.H., Froment G.F. Production of light alkanes from methanol on ZSM-5 catalyst.// Appl. Catal. 1991. v.71. - P.153-165.
Колисниченко Н.В., Яшина О.В., Маркова Н.А., Хаджиев С.Н., Китаев Л.Е. Конверсия диметилового эфира в олефины С2-С4 на цеолитных катализаторах.// Нефтехимия, 2009, т. 49, №1, -С. 45-49.
Chanq C.D., Chu C.T.-W., R.F.Socha. Methanol conversion to olefins over ZSM-5: 1. Effect of temperature and zeolyte SiO2/Al2O3. // J. Catal. 1984. v. 86. - P.289-296.
Kaeding W.W., Barile G.C.,Wu M.M. Mobil Zeolite Catalyst for Monomers // J. Catal, 1988,
-P. 114-118.
Мамедов С.Э. Селективный синтез п-ксилола на модифицированных ультрасилах.// Нефтехимия, 1998, т. 38, №1, - C. 60-64.
Мамедов С.Э., Генджалиева И.Ш.. Исследование свойств модифицированных высокодисперсных цеолитов в конверсии метанола в пара-ксилол.// ЖПХ, 2010, т.83, №6, - С. 1044-1047.
Хаджиев С.Н., Колесников Н.В. Получение низших олефинов из природного газа через метанол и его производные.//Нефтехимия, 2008, т.49, №5, - C. 323-333.
Сафонова С.С., Коваль Л.М., Чернов Е.Б., Болотов В.В. Физико-химические свойства модифицированных цеолитных катализаторов и их каталитическая активность в процессе совместной конверсии метанола и алканов С3-С4. // Журнал физической химии, 2005, т.79, № 1, - С. 55-60.
Ахлебнина А.А., Московская И.Ф., Ющенко В.В., Романовский Б.В. Каталитическое окисление метанола на высокодисперсном оксиде железа в микро- и мезопористых молекулярных ситах.// Журнал физической химии, 2006, т.80, №1, - С. 72-76.
Dessan R.M. H-ZSM-5 catalyzed formation of ethylene from methanol.// J. Catal., 1987, v.103, №2, - P.526-528.