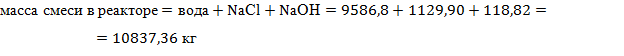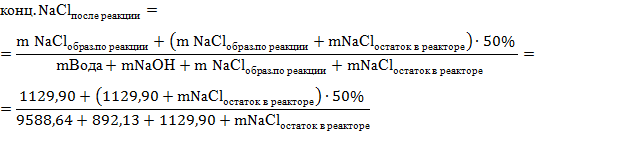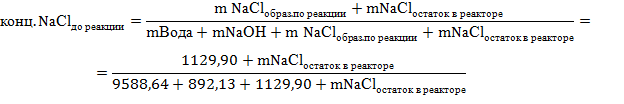Трихлорэтилен – один из основных промышленных продуктов предприятий хлорорганического синтеза. За счет высокой растворяющей способности, негорючести и незначительной токсичности он используется в различных отраслях промышленности, сфере бытового обслуживания, для наркоза и анестезии в медицине. Области применения ТХЭ продолжают расширяться, в том числе как сырья для получения разнообразных химических продуктов. Разработан ряд методов его промышленного производства, однако, благодаря своей простоте и дешевизне, метод дегидрохлорирования тетрахлорэтана 11– 18 %-ным известковым молоком используется в промышленности до настоящего времени, в том числе и на Волгоградском ВОАО «Химпром». Основной недостаток этого процесса – образование большого количества загрязненных неприятно пахнущими хлорорганическими примесями шламсодержащих сточных вод (15–25 м3/т товарного продукта). Данная проблема особенно острая для ВОАО «Химпром». Наличие в отработанном известковом молоке осадка, выступающего как адсорбент примесей, резко ухудшает экологические условия отделения шлама, приводя к загазованности отделения фильтрации интенсивно пахнущими компонентами. В составе этих примесей наряду с исходным тетрахлорэтаном и конечным ТХЭ, по данным газохроматографического анализа, определены пента- и гексахлорэтаны, а также гексахлорбутадиен и другие, в том числе не идентифицированные компоненты. Исключение образования осадка возможно при замене известкового молока на водный раствор едкого натра, в том числе за счет более высокой растворимости образующегося хлористого натрия по сравнению с хлористым кальцием. При этом, несмотря на относительное удорожание используемого щелочного агента, возможно исключение расходов на осуществление фильтрации шлама, его последующее захоронение и снижение общего количества сточных вод и, следовательно, расходов на их перекачку и биологическую очистку. Однако и в этом случае возможность многократного рецикла водно-солевого слоя будет ограничена достижением предела растворимости хлористого натрия. Хлорид натрия умеренно растворяется в воде, его растворимость мало зависит от температуры: коэффициент растворимости NaCl (в г на 100 г воды) равен 35,9 при 21 °C и 38,1 при 80 °C. Растворимость хлорида натрия существенно снижается в присутствии хлороводорода, гидроксида натрия, солей — хлоридов металлов, что нужно учитывать при расчете рецикла водно-солевого слоя.
Рассмотрим возможность осуществления рецикла водно-солевого слоя процесса дегидрохлорирования тетрахлорэтана раствором гидроксида натрия на примере производства трихлорэтилена на ВОАО «Химпром».
Синтез проводится в реакторе периодического действия, подогрев реакционной массы, а также ее перемешивание осуществляется за счет острого пара, подаваемого в реакционное пространство. Образовавшийся трихлорэтилен испаряется, за счет чего производится эффективный отвод тепла экзотермической реакции. После этого в реакторе остается водно-солевой слой, состоящий из непрореагировавшего раствора NaOH, воды и соли - продуктов реакции и воды - сконденсировавшегося пара. Этот водно-солевой возможно использовать многократно.
Рецикл организован таким образом, что водный раствор, содержащий соль хлорида натрия, находящийся в реакторе после синтеза частично сливается. Оставшаяся в аппарате водная часть, согласно данным материального баланса, доводится до исходных концентраций. Затем вновь осуществляется синтез.
Таблица 1
Материальный баланс производства трихлорэтилена для расчета рецикла водно-солевого слоя
|
Приход |
Расход |
||
|
Вещество |
Вещество |
||
|
Раствор NaOH: |
Непрореагировавший раствор NaOH: |
||
|
NaOH |
892,13 |
NaOH |
118,82 |
|
Н2О |
7300,08 |
Н2О |
7306,01 |
|
|
|
Продукты реакций: |
|
|
|
|
Н2О |
357,14 |
|
|
|
NаСl |
1129,90 |
|
|
|
||
|
Пар |
1923,68 |
Вода |
1923,68 |
|
Итого |
10115,89 |
Итого |
10837,36 |
Основываясь на данных материального баланса производства рассчитаем концентрацию NаСl в реакторе после первого цикла, для этого:
Дополнительный расчет рецикла в HYSYS показал, что необходимо слить из ректора 50% смеси, в реакторе остается, кг:
|
Вода |
4 793,4 |
|
NаСl |
564,95 |
|
NаОН |
59,41 |
|
∑ |
5 417,76 |
Концентрация NаСl в реакторе после слива 50% смеси остается равной 10,43%.
Концентрация NаОН в реакторе после слива 50% смеси:
-
Доведем массу NаОН до исходной 892,13 кг:
Доведем массу Н2О до исходной 9588,64 кг:
-
- Состав смеси в реакторе перед вторым циклом:
|
Вода |
9 586,8 |
|
NаСl |
564,95 |
|
NаОН |
892,86 |
|
∑ |
11 046,45 |
Концентрация NаСl перед вторым циклом:
-
После второго цикла образуется 1129,90 кг NаСl.
Для второго и последующих циклов концентрация NаСl рассчитывается аналогично. Однако нужно учесть накопление хлорида натрия. Выведем общее уравнение для расчета концентрации NаСl в реакторе после протекания реакции и перед ней.
-
- Сведем данные в таблицу:
Таблица 2
Накопление соли NаСl в реакторе при организации рецикла водно-солевого слоя
|
Цикл |
Концентрация NаСl, % |
Накопление NаСl, кг |
|
|
до реакции |
после реакции |
||
|
1 |
0,00 |
10,43 |
0 |
|
2 |
5,11 |
15,34 |
564,95 |
|
3 |
7,48 |
17,45 |
847,43 |
|
4 |
8,62 |
18,47 |
988,66 |
|
5 |
9,18 |
18,97 |
1 059,28 |
|
6 |
9,46 |
19,22 |
1 094,59 |
|
7 |
9,59 |
19,34 |
1 112,25 |
|
8 |
9,66 |
19,40 |
1 121,07 |
|
9 |
9,70 |
19,43 |
1 125,49 |
|
10 |
9,71 |
19,45 |
1 127,69 |
|
11 |
9,72 |
19,45 |
1 128,80 |
|
12 |
9,73 |
19,46 |
1 129,35 |
|
13 |
9,73 |
19,46 |
1 129,62 |
|
14 |
9,73 |
19,46 |
1 129,76 |
|
15 |
9,73 |
19,46 |
1 129,83 |
|
16 |
9,73 |
19,46 |
1 129,87 |
|
17 |
9,73 |
19,46 |
1 129,88 |
|
18 |
9,73 |
19,46 |
1 129,89 |
|
19 |
9,73 |
19,46 |
1 129,90 |
|
20 |
9,73 |
19,46 |
1 129,90 |
Как видно по данным таблицы 2, начиная с 12 цикла, накопление NaCl переходит в стационарный режим. Концентрация соли не превышает 20%, что говорит о том, что в данных условиях соль в осадок не выпадает. Следовательно, возможно организовать рецикл водно-солевого слоя с неограниченным количеством циклов.
Проведенный расчет показал, что совершенствование способа получения трихлорэтилена путем замены щелочного агента на раствор гидроксида натрия и организация рецикла водно-солевого слоя позволило избежать образования большого количества загрязненных неприятно пахнущими хлорорганическими примесями шламсодержащих сточных вод. Рецикл дал возможность более полного использования дорогостоящего щелочного агента, обеспечил сокращение количества сточных вод в два раза без ухудшения их качества.
- Литература:
1. Промышленные хлорорганические продукты: справочник / под ред. Л. А. Ошина. – М.: Химия, 1978. – 656 с.
2. Трегер, Ю. А. Основные хлорорганические растворители / Ю. А. Трегер, Л. М. Карташов, Н. Е. Кришталь. – М.: Химия, 1984. – 224 с.
3. Муганлинский, Ф. Ф. Химия и технология галогенорганических соединений / Ф. Ф. Муганлинский, Ю. А. Трегер, М. М. Люшин. – М.: Химия, 1991. –272 с.
4. Кабердин, Р. В. Трихлорэтилен в органическом синтезе / Р. В. Кабердин, В. И. Поткин // Успехи химии. – 1994. – № 8. – Т. 63. – С. 673–692.
5. Ускач Я. Л., Зотов С. Б., Попов Ю. В.Совершенствование технологии получения трихлорэтилена.- Волгоград: Известия ВолгГТУ, 2009.-С. 93-96.