Рассеянный склероз – хроническое прогрессирующее заболевание, характеризующееся множественными очагами поражения в центральной и в меньшей степени периферической нервной системе. В большинстве случаев рассеянный склероз дебютирует в возрасте от 20 до 40 лет, чаще болеют женщины. В мире рассеянным склерозом страдают около 2 млн. человек, в том числе в России примерно 150000 [2, с.43]. В последние годы отмечается рост показателей заболеваемости РС, что связано не только с усовершенствованием методов диагностики, но и с абсолютным ростом числа заболевших [6,с.13]. Общепринято, что РС – мультифакториальное заболевание, развитие которого обусловлено взаимодействием факторов внешней среды (вируса и географических факторов) и наследственной предрасположенности [6, с.11; 14, с.268], что обеспечивает вариабельность патологии, ее фенотипического проявления, течения и исходов. Однако, несмотря на многолетние исследования, причины возникновения этого демиелинизирующего заболевания остаются не до конца изученными [4, с.18]. То же самое можно сказать и о факторах, влияющих на течение и степень прогрессирования заболевания. Считается, что генетические факторы, видимо, в большей степени влияют на заболеваемость РС, а средовые – на его клиническое течение [13]. В исследованиях возможных «внешних» факторов развития РС установлена связь этого заболевания с преобладанием в диете животных белков и жиров, хронической интоксикацией органическими растворителями, бензином, металлами и другими веществами, хроническими психо-эмоциональными стрессами, курением, особенностями микроэлементарного состава почвы, недостатком солнечного света (дефицит витамина D), [3, с.9; 6, с.19-20]. В роли пускового механизма заболевания могут выступать различные факторы, в том числе вирусные агенты и микроорганизмы [10, с.430-435;16]. Доказано, что максимальная активация заболевания происходит в течение 2 недель от начала инфекции [16]. Таким образом, интересно, влияет ли наличие сопутствующих хронических заболеваний на течение и скорость прогрессирования РС. Ведь большинство хронических заболеваний связаны с наличием в организме инфекционных агентов и изменением иммунного статуса, в том числе образованием аутореактивных клеток и продукцией большого количества провоспалительных цитокинов. Как известно, ключевую роль в патогенезе РС играют Th-1 и Th17 лимфоциты, аутоагрессивные по отношению к миелину ЦНС [5, с.60;16]. Таким образом, наличие хронического очага воспаления в организме может способствовать активации воспалительного процесса в мозге.
Целью нашего исследования являлось изучение влияния сопутствующей соматической и аутоиммунной патологии на течение РС на территории Омской области.
Материал и методы
В соответствии с целью и задачами работы обследовано 265 пациентов с достоверным диагнозом «рассеянный склероз» по критериям McDonald, 2005 [4, с.37-39]. Для установления соответствия этим критериям анализировались данные анамнеза и снимки МРТ в динамике, предоставляемые пациентами. Тип течения заболевания уточнялся при непосредственном сборе анамнеза во время осмотра, а также на основании изучения данных амбулаторных карт, истории болезни предыдущих поступлений. Критерии включения: достоверный диагноз по критериям McDonald; письменное согласие на участи в исследовании. Критерии исключения: невозможность однозначно оценить правильность диагноза, несмотря на соответствие критериям McDonald, принадлежность к неевропеоидной расе.
Осмотр пациентов осуществлялся, при получении предварительного устного согласия, на дому, в условиях поликлиники по месту жительства, в Омской областной клинической больнице проводился осмотр пациентов, поступавших для курса лечения. После подписания пациентом информированного согласия заполнялась подробная анкета, включающая паспортную часть, анамнестические сведения, а также данные лабораторных и инструментальных методов исследования, подтверждающие диагноз, данные неврологического осмотра. Анкета заполнялась на основании слов пациента, данных амбулаторной карты или иных предоставленных медицинских документов. Данные неврологического статуса фиксировались непосредственно на момент осмотра. Неврологическое обследование проводилось по общепринятой методике с использованием шкалы неврологического дефицита Куртцке для оценки нарушений основных неврологических функций. Суммарный неврологический дефицит определялся в соответствии со шкалой EDSS [4, с.74], средняя скорость прогрессирования высчитывалась как отношение EDSS к длительности заболевания в годах. Выделяли 3 темпа прогрессирования: медленный темп - менее 0,25 б/г, умеренный – ≤0,25-0,75 б/г, быстрый – ≥0,75б/г. [1]. Число обострений симптомов заболевания отмечалось в расчете на один год.
Обследовано 265 пациентов, все пациенты были разделены на 3 группы соответственно типу течения заболевания: 148 (55,8%) пациентов с ремиттирующим типом течения, 85 (32,07%) – с вторично-прогрессирующим и 32 (12,07%) – с первично-прогрессирующим типом течения заболевания. Прогрессирующий с обострениями тип выявлен не был. Средний возраст больных составлял 27,6±11,6 лет. Пациенты в исследуемых группах были сопоставимы по возрасту и морфологическим показателям – росту и весу (Табл. 1).
Таблица 1
Общая характеристика больных в исследуемых группах
|
|
Ремиттирующий (n=148) М ± SD
|
Вторично-прогрессирующий (n=85) М ± SD |
Первично-прогрессирующий (n=32) М ± SD |
|
Возраст, лет |
35,25±12,26 |
40,76±10,16 |
41,43±12,2 |
|
Рост, см |
168,55±7,84 |
168,55±7,84 |
167,97±7,41 |
|
Вес, кг |
67,07±12,74 |
67,07±12,74 |
66,46±14,99 |
Статистическая обработка проводилась с помощью программы Statistica 6.0 фирмы StatSoft и MIX для Windows, а также возможностей Microsoft Excel. Критическое значение уровня статистической значимости при проверке нулевых гипотез принималось равным 0,05. Проверка нормальности распределения вероятности количественных признаков с помощью критерия Колмогорова и критерия Шапиро-Уилки, показала, что все количественные признаков в группах сравнения не имели нормального распределения [7, c.77,83]. Поэтому для сравнения центральных параметров групп использовались непараметрические методы: дисперсионный анализ Краскела-Уоллиса с ранговыми метками Вилкоксона и критерий Ван дер Вардена, сравнение двух независимых групп выполнялось с помощью U-теста Манна-Уитни. Для всех количественных признаков в сравниваемых группах производилась оценка медианы и стандартного отклонения, а также интерквартильного размаха (25 и 75 процентили) [7,с. 109;9, с.112, 125, 129].
Результаты и обсуждение
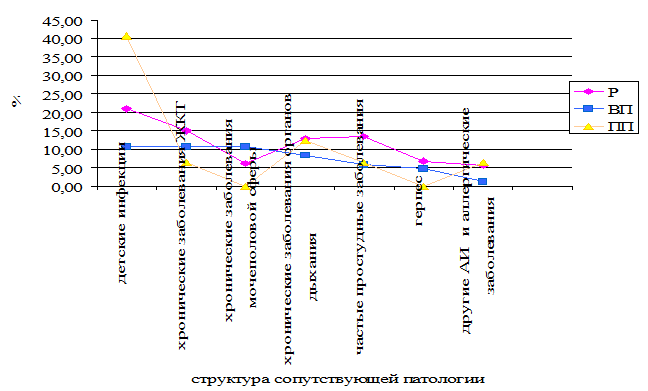
Первой задачей проведенного исследования было изучение особенностей клинических проявлений рассеянного склероза в зависимости от наличия хронических заболеваний на территории Омской области. По данным S. Simionia и соавторов, наличие у пациентов с РС сопутствующих сосудистых заболеваний и ожирения повышает риск развития легкой нетрудоспособности [12]. С.А. Сиверцева указывает на то, что в тюменской популяции выявлена связь хронического тонзиллита, инфекционными заболеваниями глаз, половой сферы с возникновением РС [8]. Мы предположили, что хронические воспалительных заболеваний различной локализации также могут влиять на течение РС. Однако частота встречаемости хронических воспалительных заболеваний у пациентов с различными типами течения РС не отличалась (р>0,05). При анализе частоты встречаемости различных групп сопутствующих заболеваний у пациентов с разными типами течения РС установлено, что пациенты с ППРС в детстве чаще болели различными острыми инфекционными заболеваниями по сравнению с группой РРС и ВПРС (р<0,00001). Однако исследование крови на наличие антител к возбудителям детских инфекций не проводилось, данные о перенесенных инфекциях во взрослом возрасте подтверждены данными лабораторных анализов амбулаторных карт пациентов. Частота встречаемости хронических воспалительных и аутоиммунных заболеваний у пациентов с разными типами течения РС не отличалась (p>0,05 для всех сравниваемых признаков)
Рисунок 1. Структура сопутствующей патологии у пациентов в зависимости
от типа течения РС
При анализе структуры сопутствующих заболеваний было установлено, что 71 человек из 265 (26,8%) имеют сопутствующие хронические воспалительные заболевания. Структура сопутствующих заболеваний представлена в Таблице 2. Среди сопутствующих заболеваний наиболее часто отмечались заболевания ЖКТ – у 33 человек (12,45%), и органов дыхания – у 30 человек (11,32%). Заболевания мочеполовой системы зафиксированы у 18 пациентов (6,79%), рецидивирующая герпетическая инфекция – у 14 человек (5,2%). При этом всего 27 человек (10,2%) считают себя часто болеющими простудными заболеваниями (ОРЗ и ангины). Многими исследователями подтверждено, что РС имеет ряд общих локусов с другими аутоиммунными заболеваниями [11, с.5;18,с.11-14;15]. Однако сопутствующие аутоиммунные заболевания отмечены только у 8 человек (3,02%) и включали бронхиальную астму, гломерулонефрит, аутоиммунный тиреоидит, ревматоидный артрит. Таким образом, пациентов в исследуемой выборке нельзя отнести к часто болеющим простудными заболеваниями или сочетанной аутоиммунной патологией. У большинства обследованных пациентов (194 человека (73,2%)) единственным хроническим заболеванием является рассеянный склероз. При опросе и анализе медицинской документации пациентов с РС не вывялено у них сочетания РС с системными заболеваниями.
Таблица 2
Структура сопутствующей хронической воспалительной и аутоиммунной патологии в исследуемой выборке
|
|
Абсолютное количество, человек |
Относительное количество, % |
|
Частые простудные заболевания |
27 |
10,19 |
|
Хронический гастрит, дуоденит |
17 |
6,42 |
|
Хронический бронхит |
15 |
5,66 |
|
Герпес |
14 |
5,28 |
|
Хронический холецистит |
13 |
4,91 |
|
Хронический тонзиллит |
9 |
3,40 |
|
Хронический панкреатит |
5 |
1,89 |
|
Аднексит |
5 |
1,89 |
|
Цистит |
5 |
1,89 |
|
Язвенная болезнь желудка и ДПК |
4 |
1,51 |
|
Гепатит |
3 |
1,13 |
|
Хронический пиелонефрит |
3 |
1,13 |
|
Простатит |
3 |
1,13 |
|
Бронхиальная астма |
3 |
1,13 |
|
Аллергии |
3 |
1,13 |
|
Хронический ларингит |
2 |
0,75 |
|
Ревматизм |
2 |
0,75 |
|
Ревматоидный артрит |
2 |
0,75 |
|
Аутоиммунный тиреоидит |
2 |
0,75 |
|
Синусит |
2 |
0,75 |
|
Гломерулонефрит |
1 |
0,38 |
|
Кольпит |
1 |
0,38 |
|
Фиброзно-кистозная мастопатия |
1 |
0,38 |
|
Мигрень |
1 |
0,38 |
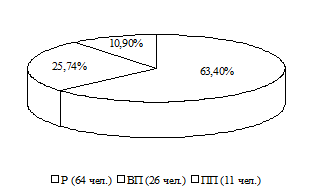
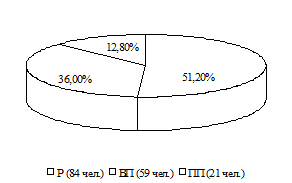
Также не установлено влияния наличия сопутствующих заболеваний на средний балл по EDSS (и при наличии, и при отсутствии соматических хронических заболеваний медиана была равна 3,5б). Длительность заболевания была выше в подгруппе пациентов с хроническими заболеваниями (медиана 8,0±7,2 года, интерквартильный интервал 4,0-14,0) по сравнению с пациентами без сопутствующих хронических воспалительных и аутоиммунных заболеваний (медиана 5,0±7,3, интерквартильный интервал 3,0-11,0), р=0,016. Также выявлены статистически значимые отличия по уровню ССП: в подгруппе пациентов, имеющих сопутствующие заболевания медиана была равна 0,75±0,8, интерквартильный интервал 0,24-0,95, в то время как в подгруппе без сопутствующей хронической патологии медиана 1,28±1,92, интерквартильный интервал 0,33-1,33; р=0,018. Однако подгруппы отличались по составу: в подгруппе пациентов часто болеющих простудными заболеваниями и имеющих хронические воспалительные заболевания больных с РРС было 64 чел. (63,4%), с ВПРС – 26 человек (25,74%), с ППРС – 11 чел. (10,9%); в подгруппе пациентов, у которых РС являлся единственным хроническим воспалительным заболеванием больных с РРС было 84 человека (51,2%), с ВПРС – 59 человек (36,0%), с ППРС – 21 человек (12,8%). Тем не менее, статистически значимых различий по составу подгрупп не получено (р>0,05).
Это может быть связано с тем, что в подгруппе пациентов, у которых РС являлся единственным хроническим заболеванием, процент пациентов с РРС был несколько ниже, а с ВВПР – выше, чем во второй подгруппе, хотя статистически значимых отличий по составу подгрупп не обнаружено. Пациенты с ВПРС, вследствие более длительного течения болезни, могут иметь больше хронических соматических заболеваний, во-первых, из-за наличия осложнений РС, таких как хронические воспалительные заболевания мочевыделительной системы у пациентов с тазовыми расстройствами, во-вторых, из-за наличия побочного действия лекарств (например, заболевания ЖКТ как следствие лечения глюкокортикостероидами). Таким образом, на наш взгляд, нельзя сделать вывод о более быстрых темпах прогрессирования у пациентов без сопутствующей патологии.
а) б)
Рисунок 2. а) Структура РС в подгруппе пациентов с сопутствующими хроническими воспалительными заболеваниями и аутоиммунными, а также часто болеющих простудными заболеваниями пациентов; б) Структура РС в подгруппе пациентов без сопутствующих хронических воспалительных и аутоиммунных заболеваний
Выводы: установлено, что наличие сопутствующих хронических воспалительных заболеваний внутренних органов не влияют на EDSS и скорость прогрессирования РС у пациентов, проживающих на территории г.Омска и Омской области. Сочетание РС и другой аутоиммунной патологии в исследуемой выборке отмечено в 3,02% случаев.
Литература:
Барабаш И.А. Варианты течения и качество жизни больных рассеянным склерозом в Амурской области. – автореф. дис. …канд. мед. наук / И.А. Барабаш ; Алтайский. гос. мед. ун-т. – Новосибирск, 2007. – 24 с
Завалишин И.А., Елисеева Д.Д. Патогенетическая терапия рассеянного склероза // Лечащий врач. – 2009. – №9. – С.43-46.
Качура Д.А., Спирин Н.Н., Бойко А.Н. Экологические аспекты рассеянного склероза // Consilium-medicum. – 2008. – Т.10, №7. – с.9-14
Клиническая картина, диагностика и лечение рассеянного склероза / Под. Ред. Ф.А. Хабирова, А.Н. Бойко. – Казань: Медицина, 2010. – 88с.
Л.В. Пичугина, Б.В. Пинегин. Внутриклеточные цитокины: проблема детекции и клиническое значение // Иммунология. – 2008, №1. – С.55-63
Рассеянный склероз: диагностика, лечение, специалисты / под ред.И.Д. Столярова, А.Н. Бойко. - СПб.: ЭЛБИ-СПб, 2008. -320с.
Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. – М.: Медиа Сфера, 2002. –312с.
Сиверцева С.А. Эпидемиологические и иммунологические особенности рассеянного склероза в Тюменском регионе : автореф. дис. …докт. мед. наук / С.А. Сиверцева; Рос. Гос. мед. ун-т. – Москва, 2009. – 43 с.
Халафян А.А. STATISTICA 6. Статистический анализ данных. 3-е изд. Учебник – М.: «Бином-Пресс», 2008. – 512с.
Association between human herpesvirus 6 and occurrence of multiple sclerosis among Jordanian patients / M. Ahram, A. El-Omar, Y. Baho3 et.al.// Acta Neurologica Scandinavica. – 2009. – Vol.120. – P.430-435.
CD226 Gly307Ser association with multiple autoimmune diseases: Author manuscript / Jason P Hafler, Lisa M Maier, Jason D Cooper, et. al.// Genes and Immunity. – 2009. – N10 (1). – P. 5 – 10.
Comorbidity delays diagnosis and increases disability at diagnosis in MS / R.A. Marrie, R. Horwitz, G. Cutter, et.al. // Neurology. – 2009. – Vol.72. – P.117–124
Douglas S. Goodin. The Causal Cascade to Multiple Sclerosis: A Model for MS Pathogenesis [Electronic resourse]. – 2009. – Vol. 4, N2. – Режим доступа: http:// www.plosone.org. – [Дата обращения 09.08.2009].
Ebers G.C . Environmental factors and multiple sclerosis // Lancet Neurology. – 2008. – Vol. 7, P.268–277.
IL2RAGenetic Heterogeneity in Multiple Sclerosis and Type 1 Diabetes Susceptibility and Soluble Interleukin-2 Receptor Production [Electronic resourse]/ Lisa M. Maier, Christopher E. Lowe, Jason Cooper, et. al. – 2009. – Vol. 5, N1. – Режим доступа: http:// www.plosgenetics.org. – [Дата обращения 09.08.2009].
Jeffrey I. Greenstein. Current Concepts of the Cellular and Molecular Pathophysiology of Multiple Sclerosis [Electronic resourse] // Developmental Neurobiology. – 2006. – Режим доступа: http:// www.interscience.wiley.com.
Maria Ban. The expanding genetic overlap between multiple sclerosis and type 1 diabetes: Author manuscript // Genes and Immunity. – 2009. – N10 (1). – P. 11 – 14.