Резюме
Эритроцитарные групповые антигены крови представляют собой генетически твердое детерминированное своеобразие. Их особенности имеют многостороннее биологическое и медицинское значение. Основное значение эритроцитарных групповых антигенов ассоциируется с иммунными своеобразиями. Групповые антигены неоднородно ассоциируются при различных патологиях.
Мы изучили связь между некоторыми эритроцитарными антигенами и туберкулезом лёгких. Работа выполнена в Иммуногенетической лаборатории в Батумском Государственном Университете.
Материалами исследования служили пробы крови (эритроциты, сыворотки) 100 больных туберкулезам (79 мужчин и 21 женщина). Для оценки частоты антигенов эритроцитов среди больных в качестве контрольной группы использована популяция здоровых лиц. В работе использованы общепринятые методы иммуносерологического исследования эритроцитов и сывороток крови.
Исходя из итогов исследования, можем отметить, что носители групп O(I) и B(III) весьма чувствительны к туберкулезу легких, а носители группы A(II) сравнительно меньше подвержены этому заболеванию. Вес носителей фенотипной группы O(I) значительно выше при острой форме заболевания. Подобный результат был зафиксирован и в случаях группы B (III) фенотипа. При острой форме B(III) фенотип встречается в 3 раза больше по сравнению с донорами. У больных туберкулезом легких мужчин и женщин наблюдается варьирование концентраций D и d аллелей. В частности, оказалось, что в мужчинах концентрация D аллели 0,62, а женщинах - 0,53. В популяции больных концентрация cde гаплотипа равно 0,41, тогда как в донорской популяции она составляет 0,36. Среди больных концентрация CDE гаплотипа равно 0,01. Отмеченный гаплотип не был выявлен в донорах и он явно ассоциируется с заболеванием. Концентрация cDe и cDE гаплотипов выше в донорах. Это подтверждает, что лица, носители отмеченных гаплотипов, сравнительно менее подлежат заболеванию и характеризуются иммунной стойкостью.
Определенная ассоциативная связь была зафиксирована среди больных и доноров по своеобразиям распространения фенотипов MN группы. Большинство больных туберкулезом легких (72±4,8%) является носителем M антигена, что объясняется чувствительностью отмеченного антигена к заболевании. Зато в донорах сравнительно больше удельных вес N групп (21±4,07 %).
Введение
Группы крови, разделение индивидуумов одного и того же биологического вида (люди, обезьяны, лошади и др.) по особенностям крови, в основе которых лежат различия в строении эритроцитарных белков — гликопротеидов (антигени), обусловленные разными типами биосинтеза.
Эритроцитарные групповые антигены крови представляют собой генетически твердое детерминированное своеобразие [1]. Эритроцитарное антигенное своеобразие имеет многостороннее биологическое и медицинское значение.
В настоящее время выделяют около 25-ти эритроцитарных групповых систем, в которых объединены около 300 антигенов [2]. С клинической точки зрения самыми значительными являются ABO, Rh, Kell, MNSs и др. системы.
Основное значение эритроцитарных групповых антигенов ассоциируется с иммунными своеобразиями живого. Особую роль они имеют в трансфузиологии [3], эпидемиологии [4] и трансплантологии [5, 6].
Особое значение отмеченные системы имеют с точки зрения изучения генетики человека [7, 8], в особенности его популяционных своеобразий [9, 10, 11].
В литературе [12, 13, 14, 15, 16] встречаем множество материалов, подтверждающих неоднородное ассоциирование групповых антигенов крови при различных патологиях.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Работа выполнена в Иммуногенетической лаборатории в Батумском Государственном Университете (Грузия).
Материалом исследования служили пробы крови (эритроциты, сыворотки) 100 больных туберкулезам (79 мужчин и 21 женщина).
Для оценки частоты антигенов эритроцитов среди больных в качестве контрольной группы использована популяция здоровых лиц.
В работе использованы общепринятые методы иммуносерологического исследования эритроцитов и сывороток крови. Для определения антигенов системы применяли экспресс-метод с универсальным моноклональными антителами.
В работе использованы тест-системы со специфичностью анти-АВ, -В, -А, -D, -CD(G), -C, -c, -E, -Ce, -e, -K, -M, -N (OОО «Гемостандарт», Москва), стандартный 0(I), A(II), B(III) эритроциты и сыворотки.
Вычисление частоты генов АВ0 проводили, по формулам, предложенным F. Bernstein для трехаллельных генетических систем. Частоты генов 0, А и В в данном случае принято обозначать буквами r, p и q.
r = 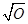 ;
;
p = 1- 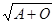 ;
;
q = 1- 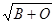
где 0, А и В – частоты лиц с группами 0(I), A(II) и B(III) в долях единицы соответственно.
Частоту генов и гаплотипов системы Rh рассчитывали, используя следующие формулы:
D = 1 - 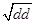 ;
;
C = 1 - 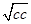 ;
;
E = 1 - 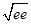 ;
;
c = 1 - 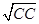 ;
;
e = 1 - 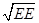
где D, C, E, c, e – частоты генов, dd, cc, ee, CC и EE – частота соответствующих фенотипов в долях единицы соответственно. Расчеты частоты гаплотипов системы Rh проводили по формулам, предложенным A. E. Mourant
cde = 
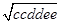 ;
;
Cde =

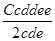 ;
;
cdE = 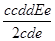 ;
;
cDe =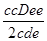 ;
;
cDE = 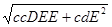 - сdE;
- сdE;
CDe =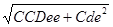 - Сde;
- Сde;
CDE=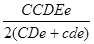
где ccddee, Ccddee, ccddEe, ccDee, CCDee и ccDEE – частота соответствующих фенотипов в долях единицы.
Частоты алелей RhD, d и K, k вычисляются следующим образом:
q = 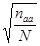 p= 1-q
p= 1-q
где 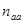 - число лиц, гомозиготных по рецессивному гену (dd da kk), N- обьем выборки.
- число лиц, гомозиготных по рецессивному гену (dd da kk), N- обьем выборки.
Вычисление частоты генов MN проводили, по формулам:
P= 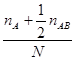 q =
q = 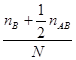
Где 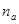 – число лиц с фенотипом M;
– число лиц с фенотипом M; 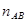 – число лиц с фенотипом MN;
– число лиц с фенотипом MN; 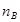 – число лиц с фенотипом N.
– число лиц с фенотипом N.
При подсчете частоты антигенов и генов учитывали ошибку по формуле: M = 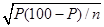 , где Р – частота антигена в %, n – количество обследованных в выборке(В. Ю. Урбах, 1975).
, где Р – частота антигена в %, n – количество обследованных в выборке(В. Ю. Урбах, 1975).
Результаты
Исходя из итогов исследования, можем отметить, что носители групп O(I) и B(III) весьма чувствительны к туберкулезу легких, а носители группы A(II) сравнительно меньше подвержены этому заболеванию. В большинстве случаев они характеризуются иммунной стойкостью (Картина 1).
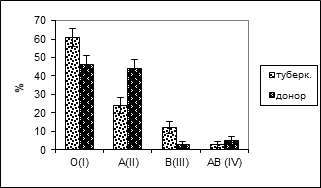
Картина 1. особенности распространения ABO фенотипов среди больных туберкулезом легких и здоровых доноров.
В больных популяциях отмечается высокая концентрация r алела по сравнению с донорской популяцией. В них незначительно высока концентрация p алела. Концентрация q алела в контрольной группе выше в 2, 14 раз.
Оказалось, что вес носителей фенотипной группы O(I) значительно выше при острой форме заболевания. Подобный результат был зафиксирован и в случаях группы B (III) фенотипа. При острой форме B(III) фенотип встречается в 3 раза больше по сравнению с донорами. Альтернативная картина зафиксирована в случае фенотипной группы A(II) (Картина 2).
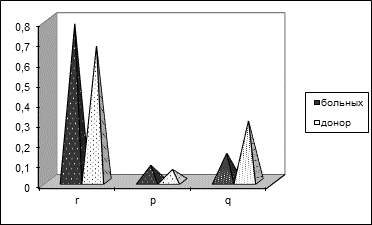
Картина 2. Особенности распространения ABO фенотипов среди больных туберкулезом легких и здоровых доноров.
В больных туберкулезом легких женщинах по сравнению с мужчинами концентрация r алела в 1,23 раза больше. Зато в больных мужчинах по сравнению с женщинами в 2,5 раза выше концентрация p алела и в 3, 16 раза - q алела (Картина 3). Это свидетельствует о большей предобусловленности мужчин по отношению к заболеванию.
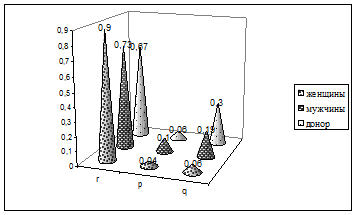
Картина 3. Концентрация r, p, q аллелей в донорах и больных туберкулезом гегких женщинах и мужчинах.
В больных туберкулезом легких выявилась высокая концентрация p(M) аллели, а концентрация q(N) аллели наоборот, выше в донорах (0,35) (Картина 4).
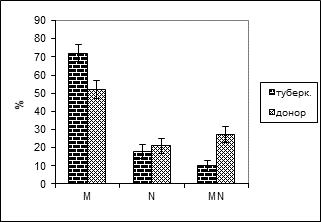
Картина 4. Частота распространения MN фенотипов в больных и здоровых популяциях.
Можно сказать, что ношение N алела представляет знак «зашиты». В носителях отмеченного алела и соответственно, носителях антигена в 1,5 раза меньше риск развития заболевания.
В популяции больных выявилась высокая частота распространения D антигена (Картина 5).
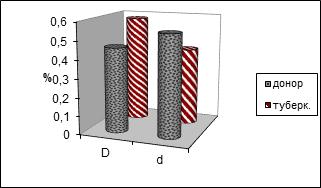
Картина 5. Концентрация D и d аллелей в больных и здоровых популяциях.
Отмеченный антиген коррелирует с туберкулезам. Это означает, что в лицах, у которых на поверхности эритроцитов экспрессирован D антиген, высока теоретическая вероятность выявления заболевания. В них по сравнению с носителями d алели в 1,05 раза больше выявляется отмеченное заболевание.
В литературе зафиксированы данные, согласно которым в лицах, имеющих D(+) существенно низок титр антибактериальных антител [17]. Интенсивность иммунного ответа, вызванная некоторыми бактериальными анатоксинами, коррелирует с D и E антигенами.
У больных туберкулезом легких мужчин и женщин наблюдается варьирование концентраций D и d аллелей. В частности, оказалось, что в мужчинах концентрация D аллели 0,62, а женщинах - 0,53 (Картина 6). Это еще раз говорит о большей зависимости мужчин от отмеченного заболевания.
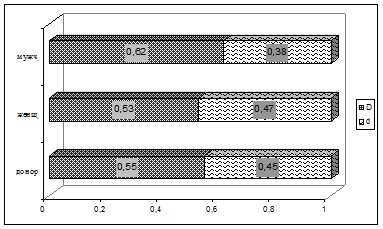
Картина 6. Концентрации D и d аллелей в мужчинах и женщинах.
У больных высокой частотой представлен СС вариант доминантного гомозиготного С гена, тогда как частота распространения гетерозиготных и рецессивных гомозиготных вариантов более высока в донорах ( Картина 7).
Положительная корреляционная связь зафиксирована между Ее генотипом и отмеченным заболеванием. ее генотип в больных и контрольных группах представлен равными процентными показателями. Носители ЕЕ генотипа оказались стойкими к заболеванию. В частности, в женщинах число носителей ЕЕ генотипа в 1,9 раза выше по сравнению с донорами, а в мужчинах - еще выше. В женщинах, носящих ЕЕ генотип, отмеченное заболевание зафиксировано в 7,5 раза больше. Противоположная картина выявилась по Ее генотипу, частота распространения которого у мужчин в 1,22 раза превосходит зафиксированный у женщин показатель (Картина 8).
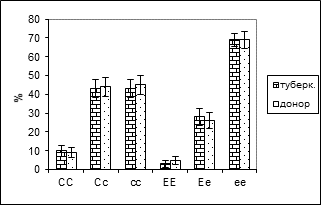
Картина 7. Частота гомо- и гетерозиготных положений в больных и здоровых популациях.
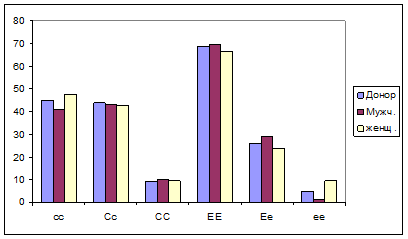
Картина 8. Своеобразия распространения СС, Сс, СС, ЕЕ, Ее, ее генотипов у представителей обоих полов, больных туберкулезом легких и доноров.
При изучении Rh фенотипов у больных выявился редкий - - Dee фенотип, который в здоровой популяции вообще не выявлялся. При отмеченном фенотипе серологично не выявляются продукты С и с кодоминантных аллелей. Надо предполагать, что ввиду каких-то причин происходит супрессия отмеченных локусов, что вызывает генетическую предрасположенность к заболеванию. Кроме того, в больной популяции, в отличие от доноров, был выявлен CCDEe фенотип, в котором одновременно встречаются три доминантных C, D, E антигенных продукта аллели (Картина 9).
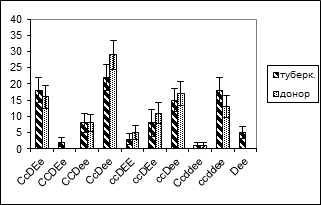
Картина 9. Частота распространения фенотипов среди больных туберкулезом легких и доноров.
В популяции больных концентрация cde гаплотипа равно 0,41, тогда как в донорской популяции она составляет 0,36. Среди больных концентрация CDE гаплотипа равно 0,01. Отмеченный гаплотип не был выявлен в донорах и он явно ассоциируется с заболеванием.
Концентрация cDe и cDE гаплотипов выше в донорах (Картина 10). Это подтверждает, что лица, носители отмеченных гаплотипов, сравнительно менее подлежат заболеванию и характеризуются иммунной стойкостью.
Определенная ассоциативная связь была зафиксирована среди больных и доноров по своеобразиям распространения фенотипов MN группы. Большинство больных туберкулезом легких (72±4,8%) является носителем M антигена, что объясняется чувствительностью отмеченного антигена к заболевании. Зато в донорах сравнительно больше удельных вес N групп (21±4,07 %). С химической точки зрения антигени MN системы относятся к гликофорину – А. Циалогликопротеин, являющийся основным лигандом некоторых бактерий и вирусов, обознается от кислоты N-ацетилнейрамина, входящей в состав этого белка (гликофорин – А). Вследствие исследования была установлена возможность влияния вариабельности генетической MN системы на бактериальную и вирусную конкуренцию [18].
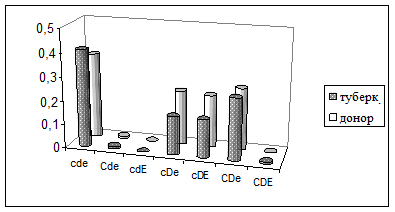
Картина 10. Концентрация Rh гаплотипов в больных и здоровых популяциях.
Применением статистических методов была вычислена концентрация p(M) и q(N) аллелей в больных и контрольных популяциях. Выявилось, что концентрация p(M) аллели выше (0,77) в больных, чем в донорах (0,66). Концентрация q(N) аллели, наоборот, выше в донорах (0,35) (Картина 11).
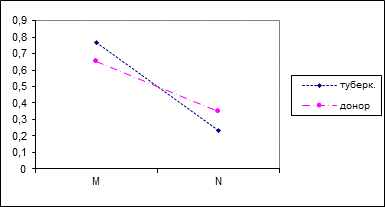
Картина 11. Концентрация М и N аллелей в больных и здоровых популяциях.
Можно сказать, что ношение N алели в какой-то мере является «защитным» знаком. В носителях отмеченного аллели и, соответственно, антигенах в 1,5 раза меньше риск развития заболевания.
Поскольку все аллоантигены представляют продукт серологические выявленного соответствующего гена, возможно с достаточно высокой точностью и к тому же перспективно изучение коррелятивной связи между эритроцитарным составом и разного вида патологией.
Исследование в этом направлении даст возможность подытожить, экспрессия какого группового антигена ассоциируется с вышеназванными патологиями. Изучением частоты распространения эритроцитарных антигенов у больных и их сравнением со здоровыми донорами станет возможным выделить индивиды высокого риска, предрасположенные к заболеванию и с целью его избежание провести профилактические мероприятия.
Список Литературы:
1. Instee O. J. Blood group active surfase molecules of the human red blood cells. Vox Sang. 1990. V. 58. P. 1-20.
2. Минеева Н.В. Современная классификация антигенов эритроцитов. Новое в трансфузиологии. 1999. №24. C. 31-38.
3. Schonewille H, van de Watering LM, Loomans DS, Brand A. Red blood cell alloantibodies after transfusion: factors influencing incidence and specificity. Transfusion. 2006;46(2):250-6.
4. Vojvodic S. Inhibitory activity of blood group antigens M and N in inhibition of virus hemagglutination reactions of influenza viruses. Med Pregl. 2000. 53(1-2):7-14
5. Bolan C. D., Leitman S. F., Griffith L. M., Wesley R. A., Procter J. L., Stroncek D. F., Barrett A.J., Childs R. W. Delayed donor red cell chimerism
and pure red cell aplasia following major ABO-incompatible nonmyeloablative hematopoietic stem cell transplantation.Blood. 2001. 98(6):1687-1694.
6. Bucin D., Johansson S., Malm T., Jogi P., Johansson J., Westrin P., Lindberg LO., Olsson AK., Gelberg J., Peres V., Harling S., Bennhagen R., Kornhall B., Ekmehag B., Kurkus J., Otto G. Heart transplantation across the antibodies against HLA and ABO. Transpl Int. 2006; 19(3):239-44.
7. Cartron JP. Defining the Rh blood group antigens. Biochemistry and molecular genetics. Blood Rev. 1994. 8(4):199-212.
8. Shubin PN., Morokov VA., Efimtseva EA., Chelpanova TI. Ethnogenetics of the Komi-Zyrians according to data on the distribution of gene frequencies of erythrocyte and serum systems in the blood. Genetika. 1997;33(2):235-42.
9. Kucher AN., Puzyrev VP., Chernetsov DB., Erdynieva LS., Sanchat NO. “Polymorphism of immunological and biochemical marker genes in rural populations of the Tuva Republic”. Genetika. 2000; 36(4):562-9.
10. Paoli G, Franceschi MG. Genetic studies in the Garfagnana population (Tuscany, Italy). Anthropol Anz. 1990;48(4):333-45.
11. Nasidze IS. Genetic polimorfisms of the Caucasus ethnic groups: Distribution of some serum protein and red cell enzyme genetic markers. Gene Geogr. 1995; 9(2):91-116.
12. Nazaretian MK., Nersisian VM., Martirosian IG., Musaelian NO., Nalian AA. Distribution of immunogenetic markers of erythrocyte systems in ischemic heart disease. Gematol Transfuziol. 1993.38(6):40-2.
13. Volkova KI., Blinetskaia ZS., Fateev IN. Genetic blood markers of the ABO system in patients with pulmonary tuberculosis in relation to ethnic origin Probl Tuberk. 1991; (10):55-8.
14. Кузнецов А. В., Епифанов Д. В., Рау И. В., Мороков В. А. Особенности распределения фенотипов и генов систем АВ0 и Rh эритроцитов крови человека среди больных некоторыми видами сосудистой патологии. Мед. наука в Республике Коми. Сыктывкар. 2000. Вып.16. С.44 - 48.
15. Su M, Lu SM, Tian DP, Zhao H, Li XY, Li DR, Zheng ZC. Relationship between ABO blood groups and carcinoma of esophagus and cardia in Chaosan inhabitants of China. World J Gastroenterol. 2001. 7:657-661.
16. Graziano SL, Tatum AH, Gonchoroff NJ, Newman NB, Kohman LJ. Blod group antigen A, and flow cytometric analysis in resected early-stage non-small cell lung cancer. Clin Cancer Res. 1997. 3:87-93.
17. Донсков С. И., Липатова И. С. Аллоиммунизация антигенами эритроцитов – глобальный популяционный процесс. Вестник службы крови России. 2001. №3. C. 18-24.
18. Bottini N., Ronchetti F., Gloria-Bottini F., Stefanini L., Bottini E., Lucarini N. Atopic and nonatopic asthma in children. J Asthma. 2005;42(1):25-8.







