Желудочковая экстрасистолия по-прежнему остается одной из самых распространённых аритмий, особенно велика её частота в популяции лиц старше 65 лет. Различные электрофизиологические аспекты возникновения данной аритмии требуют дифференцированной терапии.
Препараты аденозина (АТФ - аденозинтрифосфат) и его фосфорных эфиров (аденокард, аденокор, фосфобион) используют в клинической практике для купирования пароксизмальных наджелудочковых реципрокных тахикардий (ПНРТ), а также для дифференциальной диагностики регулярных тахиаритмий: трепетания предсердий (ТП), ПНРТ, предсердных и желудочковых тахикардий (ЖТ) [1, 6, 9].
В последние годы появились данные об эффективности АТФ при желудочковых нарушениях ритма, в частности продемонстрировано антифибрилляторное действие аденозина в экспериментах с аконитин-индуцированной аритмией. Аконитин вызывает активацию эктопических очагов возбуждения вследствие появления спонтанной деполяризации и возрастания ее скорости [18]. Данная модель по механизму развития напоминает поздние аритмии при инфаркте миокарда. В том и другом случае нарушения ритма купируются блокатором быстрого Na+-тока тетродотоксином, а также этмозином, который уменьшает Na+-ток , лидокаином и мексилетином, увеличивающими проницаемость мембран для ионов К+ [8].
Применение препаратов аденозина при желудочковых аритмиях (ЖА) описано лишь при так называемой идиопатической желудочковой тахикардии (ЖТ), возникающей у пациентов без органической патологии сердца, на фоне выраженной физической нагрузки. Доказано, что эта разновидность ЖТ обусловлена триггерной активностью, связанной с циклическим аденозинмонофосфатом, поэтому наряду с АТФ, она может быть купирована вагусными приемами и верапамилом [16].
Однако из-за фармакокинетических особенностей АТФ (при внутривенном введении болюса АТФ начало действия – приблизительно через 10сек, продолжительность эффекта – 10-20 секунд) [7], препарат не может быть применен для длительного действия, однако известен ряд препаратов, обладающих непрямым аденозинергическим действием, в частности дипиридамол (угнетает аденозиндезаминазу, а также уменьшает захват аденозина эндотелием и эритроцитами, повышая таким образом концентрацию АТФ), инозин, действующих длительно.
Цель исследования – изучение антиаритмических свойств дипиридамола при желудочковой экстрасистолии и возможность прогнозирования его антиаритмического эффекта на основе результатов фармакологической пробы с АТФ.
Материалы и методы
В исследовании приняли участие 57 пациентов в возрасте от 36 до 58 лет (средний возраст 51±1,2 лет), находившихся на стационарном лечении в кардиологическом отделении ГК БСМП г. Воронежа с нарушениями ритма по типу желудочковой экстрасистолии (ЭС). У всех пациентов по данным суточного мониторирования ЭКГ (СМ ЭКГ) регистрировалась частая желудочковая экстрасистолия - более 300 ЭС в час. Из них у 23 была выявлена ишемическая болезнь сердца, у 16– атеросклеротический стеноз устья аорты, у 7- перенесенный инфаркт миокарда. У 11 пациентов экстрасистолия носила, вероятно, функциональный характер. В исследование не включались больные с нестабильной с инфарктом миокарда давностью менее 6 месяцев, с тяжелой и злокачественной артериальной гипертензией, со стойкой артериальной гипотензией (систолическое артериальное давление (САД) < 100 мм.рт.ст.), с хронической сердечной недостаточностью ФК III-IV (NYHA), с AV-блокадой II-III степени, синдромом слабости синусового узла, бронхиальной астмой, ХОБЛ тяжёлой степени тяжести , с выраженной почечной и (или) печеночной недостаточностью, а также с другими заболеваниями или состояниями, которые могли бы повлиять на результаты исследования.
Всем обследуемым однократно проводилась внутривенная инфузия раствора АТФ 1 % со скоростью 5 мг/кг в час в течение 20 минут . Проба считалась положительной, если число ЭС снижалось более, чем на 70%, а эффект ( с учётом фармакодинамических особенностей препарата – короткого периода полувыведения) наступал в первые 5-10 минут и сохранялся более 10 – 20 минут после прекращения инфузии. Через сутки всем пациентам назначался дипиридамол (в дозе 225мг/сутки). Эффект оценивался на 3 день с помощью СМ ЭКГ (холтеровская кардиомониторная система «Кардиотехника 4000» (ОАО ИНКАРТ, СПб).
Статистический анализ полученного цифрового материала проводился на персональном компьютере с использованием статистической программы «Statgraphics». Достоверность динамики показателей определяли с помощью парного критерия t Стьюдента. За достоверность различий изучаемых параметров принимали р<0,05.
Результаты исследований
Проба с АТФ оказалась положительной у 9 больных (16%). В этой группе при приеме дипиридамола суточное количество экстрасистол уменьшилось на 50 % и более у 7 обследуемых (78%), у двоих пациентов - на 42% и 38% соответственно. Среднее количество ЭС в группе пациентов с положительной АТФ-пробой до и после приема дипиридамола до достоверно снизилось на 42,1% (рис.1) (р<0.05)
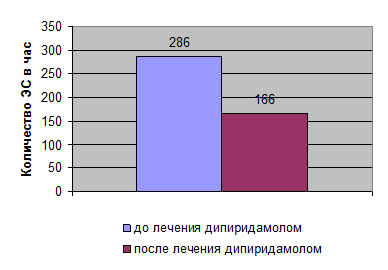
Рисунок 1. Динамика количества желудочковых экстрасистол после лечения дипиридамолом в группе пациентов с положительной АТФ - пробой (р<0.05)
В группе с отрицательной пробой уменьшение суточного количества ЭС после приема дипиридамола отмечалось лишь у 4 пациентов (8,3%) и не превышало 20%. Среднее количество ЭС по всей группе до и после приема дипиридамола достоверно не различалось (р>0,05).
Обсуждение результатов
В настоящем исследовании продемонстрирована эффективность введения АТФ и аденозинэргических препаратов при желудочковой экстрасистолии. Однако эффективность АТФ была установлена лишь у каждого 5-го пациента с желудочковой экстрасистолией. Это связано с тем, что АТФ эффективен при желудочковых нарушениях ритма определенного электрофизиологического механизма: экстрасистолии , обусловленной триггерной активностью, связанной с циклическим аденозинмонофосфатом. Процент эффективности применяемого АТФ совпадает с литературными данными о частоте встречаемости данного электрофизиологического механизма возникновения экстрасистолии.
Эффективность АТФ объясняется его непрямым (цАМФ-зависимым) и прямым (цАМФ-независимым) действием на миокард [10], которое реализуется через пуриновые (аденозиновые) Р1 (А1)-рецепторы кардиомиоцитов сократительного миокарда и проводящей системы сердца. Непрямое действие обусловлено ингибирующим действием аденозина на аденилатциклазу, активированную бета-адреномиметиками или активатором каталитической субъединицы фермента - форсколином. Хотя связь между активацией аденилатциклазы и электрической нестабильностью миокарда наблюдается не всегда [3,13,17], большинство авторов полагает, что усиление симпатического влияния на миокард, особенно на ранних стадиях ишемии, является проаритмогенным фактором.
Прямое действие аденозина на миокард обусловлено его активирующим влиянием на ацетилхолин-зависимые калиевые каналы (KACh-каналы), которые связаны с М-холинорецепторами [14] и А1-аденозиновыми рецепторами [15]. Усиление проницаемости ионов К+ через сарколемму вызывает увеличение наружу направленного К+-тока, приводящего к гиперполяризации потенциала покоя, укорочению потенциала действия, уменьшению его амплитуды и скорости деполяризации [11]. Кроме того, повышение внеклеточной концентрации К+ должно стимулировать работу Na+/K+-насоса, выводящего избыток ионов Na+ из кардиомиоцитов против градиента концентрации. Электрофизиологические эффекты аденозина и профиль его антиаритмического действия сходны с ацетилхолином, который также оказывает антифибрилляторное действие при ишемии миокарда [2, 4, 5,12].
Выводы:
1. Проведенное исследование показало высокую клиническую эффективность введения раствора АТФ, в частности установлено достоверное снижение частоты желудочковой экстрасистолии, обусловленной определенными механизмами.
2. Дипиридамол оказывает антиаритмическое действие при желудочковой ЭС определенной электрофизиологической природы.
3. Эффективность антиаритмического действия дипиридамола можно прогнозировать по результатам предварительной фармакологической пробы с АТФ.
Литература:
1. Гроер К., Кавалларо Д. Сердечно-легочная реанимация. - М.: Практика, 1996. - 125 с.
2. Елисеев В.В., Овчинникова А.Г., Евдокимова Н.Р. Антиаритмическое действие аденозина при экспериментальном инфаркте миокарда // Кардиология. - 1987. - № 7. - С.101-103.
3. Елисеев В.В., Полтавченко Г.М., Евдокимова Н.Р. и соавт. Антиаритмическое действие аденозина и содержание циклических нуклеотидов в миокарде крыс при ишемии // Бюлл.эксперим.биол. - 1987. - № 7. - С.43-45.
4. Лаун Б., Верье Р.Л. (Lown B., Verrier R.L.). Влияние парасимпатической нервной системы на стабильность электрической активности желудочков сердца // Внезапная смерть. Матер.2-го советско-американского симп. / Под ред.А.М.Вихерта, Б.Лауна. - М.: Медицина. - 1982. - С.211-226.
5. Лосев Н.А., Елисеев В.В., Крылова И.Б. Влияние холинопозитивных препаратов на развитие ранних аритмий при ишемии миокарда у крыс // Тез.докл. IV Российского национального конгресса "Человек и лекарство". - М., 1997. - С.272.
6. Медведев М.М. Использование аденозинтрифосфата для диагностики синдрома слабости синусового узла и купирования пароксизмальных наджелудочковых реципрокных тахикардий.- автореф. канд. дисс.- С-Пб, 1993.
7. Прокопенко В.М., Крылова И.Б., Елисеев В.В. Фармакокинетика аденозина у крыс // Эксперим.клинич.фармакол. - 1997. - №2. - С.56-57.
8. Розенштраух Л.В., Анюховский Е.П., Белошапко Г.Г. Уменьшение быстрого входящего натриевого тока - причина антиаритмического действия этмозина, диэтиламинового аналога этмозина, мекситила и лидокаина в поздней стадии экспериментального инфаркта миокарда // Внезапная смерть. Матер.2-го советско- американского симп. / Под ред.А.М.Вихерта, Б.Лауна. - М.: Медицина. - 1982. - С. 95- 112.
9. Сметнев А.С. Использование АТФ для купирования наджелудочковых тахикардий // Кардиология. - 1986. - №2. - С.102-103.
10. Belardinelli L., Linden J., Berne R.M. The cardiac effects of adenosine // Progr.Cardiovasc.Dis. - 1989. - Vol.32. - P.73-97.
11. Belardinelli L., Shryock J.C., Song Y. Ionic basis of the electrophysiological actions of adenosine on cardiomyocytes // FASEB J. - 1995. - Vol.9. - P.359-365.
12. Fagbemi G., Paratt J.R. Antiarrhythmic actions of adenosine in the early stages of experimental myocardial ischemia // Eur.J.Pharmacol. - 1984. - Vol.100. - P.243-244.
13. Janse M.J., Wit A.L. Electrophysiological mechanisms of ventricular arrhythmias resulting from myocardial ischemia and infarction // Physiol.Rev. - 1989. - Vol.69. - P.1049-1169.
14. Koumi S., Wasserstrom J.A. Acetylcholine-sensitive muscarinic K+ channels in mammalian ventricular myocytes // Am.J.Physiol. - 1994. - Vol.266. - P.H1812- H1821.
15. Kurachi Y., Nakajima T., Sugimoto T. On the mechanism of activation of muscarinic K+ channels by adenosine in isolated atrial cells: involvement of GTP-binding proteins // Pfluegers Arch. - 1986. - Vol.407. - P.264-274.
16. Lubbe W.F., Nguyen T., West E.J. Modulation of myocardial cyclic AMP and vulnerability to fibrillation in the rat heart // Fed.Proc. - 1983. - Vol.42. - P.2460-2464.
17. Manning A.S., Kinoshita K., Buschmans E., et al. The genesis of arrhythmias during myocardial ischemia. Dissociation between changes in cyclic adenosine monophosphate and electrical instability in the rat // Circ.Res. - 1985. - Vol.57. - P.668-675.
18. Winslow E. Methods for the detection and assessment of antiarrhythmic activity // Pharmacol.Ther. - 1984. - Vol.24. - P.401-433.







