Исследованы растворимые сополимеры на основе малеинового ангидрида и винилацетата (МА-ВА,МА-ВА-ПАСК,МА-ВА-4ААП) в качестве маскирующего вещества. Маскирующее действие сополимеров изучали при определении Cu2+ в присутствии La3+. Установлено, что сополимеры не разрушает комплекс Cu2+ с КО до 200мг/мл Cu2+,но практически полностью разрушает комплекс La3+ с КО при этих же условиях. Установлено, что они полностью маскируют ионы La3+ при определении ионов Cu2+ и можно с помощью этих сополимеров устранить постороннее воздействие La3+ для определения Cu2+ в медных сплавах.
Водорастворимые полимеры благодаря удачному сочетанию физико-химических свойств завоевали прочное положение во многих областях науки и техники. Применение их не вызывает загрязнения окружающей среды. Наибольшей практической ценностью обладают водорастворимые полимеры с комплексообразующими группами, способные образовывать устойчивые хелатные комплексные соединения с ионами металлов.[1,8]
Известно, что в составе сплавов, руд и других природных материалов наряду с ионами определяемого металла присутствуют, и другие ионы которые создают определенные трудности для точного определения этих металлов. Поэтому, необходимо устранить мешающее действие одних ионов при определении других. Эту задачу можно решить путем подбора соответствующего реагента и условий анализа. Однако в большинстве случаев это превращает анализ в многостадийный процесс. Аналогичную задачу можно решить с помощью маскирующих веществ. На практике аналитической химии применяют различные низкомолекулярные маскирующие вещества. С целью расширения круга этих веществ нами было исследовано маскирующее действие полимерного комплексообразователя. Выбор полимерного комплексообразователя в качестве маскирующих веществ связано с тем, что по сравнению с соответствующими низкомолекулярными аналогами в этих соединениях имеется высокая локальная концентрация функциональных групп и поэтому они проявляют более сильное комплексообразующее действие. [2,6]
Ранее нами были установлено, что для этого сополимеров константа устойчивости комплексов ионов трехвалентных металлов на 3-5 порядка больше константы устойчивости комплексов ионов двухвалентных металлов. Поэтому маскирующее действие полимерных комплексообразователей мы изучали при определении двухвалентного металла в присутствии трехвалентного металла.
Как известно, лантан является легирующей добавкой для улучшения механических свойств сплавов на основе кобальта, цинка и меди, входит в состав различных катализаторов. Присутствие лантана оказывает мешающее действие на определения этих металлов. Поэтому возникает необходимость маскирования ионов лантана(III).
Экспериментальная часть
В качестве полимерных маскирующих веществ были исследованы растворимые сополимеры малеинового ангидрида и винилацетата (МК-ВА). Для сравнения в качестве низкомолекулярных маскирующих веществ были использованы трилон Б и янтарная кислота.
Сополимер малеинового ангидрида с винилацетатом (МА-ВА) получили гетерогенной сополимеризацией этих мономеров в растворе[3]. Модификацию растворимых сшитых сополимеров проводили с помощью п-аминосалициловой кислоты (МА-ВА-ПАСК),4-амино-антипирином (МА-ВА-4ААП).
Исходные растворы меди и лантана с концентрацией 1×10-1М готовили растворением точных навесок CuSO4×5H2O и La(NO)3 в дистиллированной воде. В качестве фотометрического реагента для определения меди и лантана использовали водный раствор ксиленолового оранжевого (КО)[6].
В начале было изучено влияние полимерных комплексообразователей на оптические свойства комплекса ксиленового оранжевого (КО) с ионами лантана и меди. Изучение маскирующего действия полимеров при определении двухвалентного иона меди в присутствии лантана(Ш) проводили по следующей методике: в мерные колбы емкостью 25 мл вводили 5 мл буферного раствора с рН6, соответствующего количества 1·10-3 М раствора соли лантана (Ш),0,1 мл 10-2 М раствора полимеров и различные количества раствора меди,1 мл 1·10-3 М раствора КО и доводили буферным раствором с рН 6 до метки. После перемешивания измеряли оптическую плотность раствора в условиях построения градуировочного графика. По градуировочным графикам находили концентрации определяемого иона. Необходимо отметить, что в отсутствии маскирующих полимеров оптическая плотность системы в присутствии лантата(Ш) сильно отличается от значений оптической плотности в соответствующих точках градуировочного графика для определения Cu. Данные по определению Cu(II) в присутствии La(III) контролировались методом атомной абсорбции.
Результаты и их обсуждение
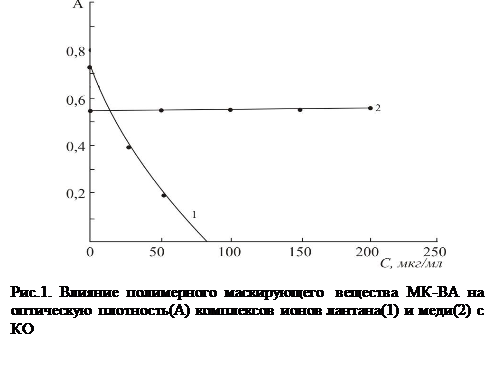
Установлено, что вышеуказанные полимеры не влияют на оптическую плотность комплекса Cu(II) с КО при концентрациях до 200мг/мл, т.е. не разрушают этот комплекс. Однако комплекс ионов лантана в этих условиях практически полностью разрушается. (рис.1).
 |
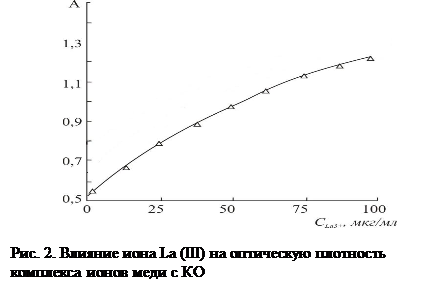
Янтарная кислота при концентрациях до 200мг/мл не влияет на оптическую плотность комплексов КО с ионами La(III) и Cu(II).Трилон Б наоборот частично разрушает все вышеуказанные комплексы. Мешающее действие ионов La(III) на определение иона Cu(II) зависит от концентрации ионов La(III) (рис.2), поэтому возникает необходимость маскирование ионов La(III) при определении вышеуказанных металлов.
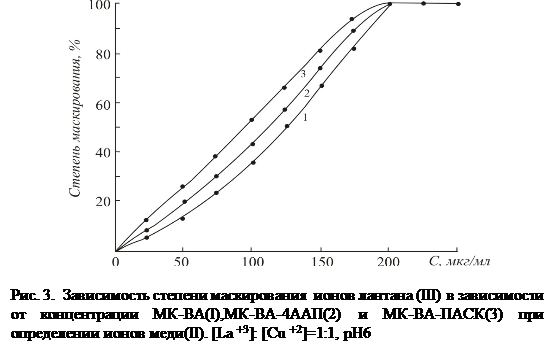 За меру эффективности действия маскирующих полимеров нами было принято приближение оптической плотности в присутствии мещающих ионов к исходному значению оптической плотности комплексов в зависимости от концентрации этих веществ. Результаты представлены в виде процента маскировки в зависимости от концентрации полимеров (рис.3).
За меру эффективности действия маскирующих полимеров нами было принято приближение оптической плотности в присутствии мещающих ионов к исходному значению оптической плотности комплексов в зависимости от концентрации этих веществ. Результаты представлены в виде процента маскировки в зависимости от концентрации полимеров (рис.3).
Как видно из рисунков при увеличении концентрации маскирующих веществ до 180-200 мг/мл удается полностью маскировать мешающее действие лантана на определении ионов Cu(II). Определение ионов Cu(II) в присутствии лантана(III) с применением полимерных маскирующих веществ представлены в табл. 1.
Таблица 1
Результаты фотометрического определения ионов Cu(II) в присутствии La(III)
при использовании полимеров в качестве маскирующего агента
Реагент –КО, рН 6, 540 нм. n = 5, P=0,95
|
Введено Cu(II),мкг/25 мл |
Соотношение Cu(II) : La (III) (мольное) |
Найдено Cu(II),мкг/25мл х ± Δ`х |
Sr |
|
МК - ВА |
|||
|
6,4 |
1:5 |
6,48 ± 0,36 |
0,037 |
|
12,8 |
2:5 |
12,70 ± 0,41 |
0,028 |
|
25,6 |
4:5 |
25,69 ± 0,49 |
0,020 |
|
32,0 |
1:5 |
31,94 ± 0,61 |
0,014 |
|
МК – ВА-4ААП |
|||
|
6,4 |
1:5 |
6,34 ± 0,36 |
0,041 |
|
12,8 |
2:5 |
12,86 ± 0,41 |
0,034 |
|
25,6 |
4:5 |
25,68 ± 0,49 |
0,022 |
|
32,0 |
1:5 |
31,95 ± 0,61 |
0,015 |
|
МК – ВА –ПАСК |
|||
|
6,4 |
1:5 |
6,35 ± 0,31 |
0,028 |
|
12,8 |
2:5 |
12,72 ± 0,35 |
0,023 |
|
25,6 |
4:5 |
25,56 ± 0,42 |
0,018 |
|
32,0 |
1:5 |
32,08 ± 0,55 |
0,011 |
Из таблицы 1 видно, что МК-ВА полностью маскируют мещающие ионы La(III) при определении ионов Cu(II). По маскирующее действие полимеров падает в ряду: МК-ВА-ПАСК>МК-ВА-4ААП >МК-ВА
Этот ряд совпадает значениями константами устойчивости этих полимеров с лантаном, чем больше константы устойчивости комплексов лантата с указанными полимеровми, тем больше маскирующее действие полимеров (Табл.2). [4,5]
Таблица 2
Логарифмы условных констант устойчивости полимерметаллических комплексов при рН 6
|
Металлы Полимеры |
La3+ |
Cu2+ |
|
МК –ВА |
10,28 |
6,81 |
|
МК– ВА – 4ААП |
10,93 |
7,23 |
|
МК –ВА – ПАСК |
10,95 |
7,34 |
В аналогичных условиях низкомолекулярные маскирующие вещества оказались малоэффективными по сравнению с полимерным комплексообразователем. Преимущества сополимеров, по-видимому, связаны с высокой локальной концентрацией функциональных групп, а значит и более сильным комплексообразующим свойствам [9].
литература
1. Осипова Е.А. Водорастворимые комплексообразующие полимеры // Соросовский образовательный журнал, 1999, №8, с. 40-47.
2.Кичигин О.В.Вестник ВГУ,2005,№1,с.46-48
3.Мамедова С.Ш., Ханларов Т.Г. и др. Авторское свидетедьство №143869,1988
4.Инцеди Я. Применение комплексов в аналитической химии. М.: Мир, 1979, 376с.
5.Gregor H.P., Luttinger L.B., Loeble E.M. Metalpolyelectrolyte complexes I.The polyacrylic acid-copper complex // Journal Phys.Chem., 1995, v.59, No.1, p.34
6.С.Б.Саввин,С.Н.Штыков,А.В.Михайлова,Органические реагенты в спектрофотометрических методах анализа. Журнал “Успехи химии”,2006,75(4),с385-389.
7.. Новые материалы. Под научной редакцией профессора Ю.С. Карабасова, Москва ,Мисис, 2002,,736 стр
8. Мясоедова Г.В., Саввин С.Б. Хелатообразующие сорбенты. М.: Наука, 1984, 173 с
9.Куренков В.Ф.Химия высокомолекулярных соединений. Казань, Изд-во редакция “Бутлеровские сообщения”,2004,146с.







