Под нашим наблюдением находилось 3434 больных с желчекаменной болезнью (ЖКБ), хроническим холециститом (ХХ) и острым холециститом (ОХ), которым было проведены эндохирургические вмешательства. Данные включают материалы отделения эндохирургии НХЦ за период с 1996 по 2014 годы. Их распределение по полу и возрасту дано в таблице 1.
Таблица 1
Распределение больных по полу ивозрасту
|
Пол |
Всего |
Возраст |
||||||
|
абс. |
% |
<20 |
21–30 |
31–40 |
41–50 |
51–60 |
>60 |
|
|
Муж. |
489 |
14,2 |
2 |
16 |
85 |
122 |
95 |
169 |
|
Жен. |
2945 |
85,8 |
30 |
240 |
523 |
684 |
628 |
840 |
|
Всего |
3434 |
100 |
32 (0,9 %) |
256 (7,5 %) |
608 (17,7 %) |
806 (23,5 %) |
723 (21,1 %) |
1009 (29,3 %) |
Как видно из таблицы 1, мужчин составили 14,2 %, а женщин — 85,8 %. Если рассмотреть возрастной аспект, то в возрасте до 20 лет было 32 (0,9 %) больных, в возрасте от 30 до 60 лет — 2137 (62,2 %).
Лиц старше 60 лет составили 29,3 % (1009 больных). 21,1 % больных составили лица в возрасте от 50 до 60 лет. Более ½ части больных составили больные в возрасте <50 лет.
Как видно из таблицы 2 ОХ был у 2671 (77,8 %) больных, из них с калькулезным проявлением — у 2656 (77,3 %) больных. Бескаменный ОХ встречался у 15 (0,5 %) больных пожилого и старческого возраста. ХХ встречался у 763 (22,2 %) больных.
Таблица 2
Распределение больных по форме холецистита
|
Формы холецистита |
Количество больных |
|
|
абс. |
% |
|
|
Калькулезный ХХ |
763 |
22,2 |
|
Калькулезный ОХ |
2656 |
77,3 |
|
Бескаменный ОХ |
15 |
0,5 |
|
Итого |
3434 |
100 |
Таким образом, по нашим данным ЛХЭ при ОХ проводилось 3,5 раза чаще, нежели при ХХ. Между тем, в течение ряда лет истории лапароскопической хирургии ОХ относился к противопоказаниям к ЛХЭ. Очевидно то, что ЛХЭ при ОХ всегда относился к категории «трудной» ЛХЭ.
Распределение больных по форме ОХ представлено в таблице 3.
Таблица 3
Распределение больных по форме ОХ
|
Форма |
Количество больных |
|
|
абс. |
% |
|
|
Катаральный |
574 |
21,5 |
|
Флегмонозный |
1788 |
66,9 |
|
Гангренозный |
309 |
11,6 |
|
Итого |
2671 |
100 |
Как видно из таблицы 3. 574 (21,5 %) больных были оперированы пло поводу катарального ОХ, 1788 (66,9 %) — флегмонозного ОХ, 309 (11,6 %) — гангренозного ОХ. Таким образом, деструктивные формы ОХ было у 2097 больных, что составляет 78,5 %. В этой таблице обращает на себя внимание достаточно большой опыт использования ЛХЭ при гангренозной форме ОХ (11,6 %). Насколько оправдан применение ЛХЭ при этой форме заболевания?
Как известно, эффективность любого эндохирургического метода зависит от опыта хирурга, практических наработок эндохирургической бригады. В этой связи, в зависимости от этапа освоения и внедрения ЛХЭ в НХЦ все оперированные нами пациенты были распределены на две клинические группы.
В контрольную группу вошли 1446 больных (54,1 %) ОХ, оперированные в период 1996–2004 годы. В указанный период шло активное освоение методов ЛХЭ, выработка оптимальных сроков операции, пересматривались показания и показания.
В основную группу вошли 1225 больных (45,9 %) ОХ, оперированные в период 2005–2015 годы. В указанны период хирургическая бригада уже в достаточной степени овладела и отточила свое мастерство при выполнении ЛХЭ.
Имея определенный опыт и собственные теоретические разработки хирургическая бригада во главе академика М. М. Мамакеева выработала тактику применения «трудных» ЛХЭ.
Мы провели анализ результатов ТЭХ в контрольной группе. Как было нами указано выше, ЛХЭ при ОХ была выполнена 1446 больным (мужчин — 17,9 %, женщин — 82,1 %). 42 % больных были в возрасте старше 60 лет, в том числе 11 % — старше 70 лет.
У 30 % больных указанной группы имелись тяжелые сопутствующие заболевания (болезни сердца, органов дыхания, ожирение, сахарный диабет и др.). У 7 женщин ЛХЭ выполнена при сроках беременности 20–24 недель.
При поступлении на основании клиники и УЗИ ставились показания к экстренной операции или проводилось медикаментозное лечение в течение 12–24 часов. Больных с бескаменным ОХ было 15 (0,5 %). Нами выработаны строгие показания к ЛХЭ у данной группы больных:
1) часто рецидивирующий болевой синдром, не поддающееся введению спазмолитиков и когда холецистографически у них было доказано нарушение эвакуации желчи из ЖП;
2) отсутствие других заболеваний органов брюшной полости и малого таза, которые могли бы симулировать ОХ;
3) отсутствие патологических отклонений в нервно-психическом статусе больного.
Нами при ОХ разработана хирургическая тактика, предусматривающая проведение консервативной терапии на протяжении 3–5 часов с момента поступления больного в клинику. В этот срок выполняем диагностические мероприятия (лабораторное, УЗИ, определение функционального состояния жизненно важных органов и систем, др.).
В последующем преобладающему большинству больных выполняется лапароскопическая диагностика, которая позволяет выявить степень выраженности морфологических изменений в стенке ЖП, определить возможность выполнения ЛХЭ.
Считаем ЛХЭ приоритетной для больных старших возрастных групп ввиду меньшей ее травматичности и других преимуществ перед ТХЭ. Оперативные вмешательства выполняли независимо от сроков, прошедших с начала заболевания.
В день госпитализации всем больным выполнена ультразвуковая и лапароскопическая диагностика. При этом у 72,7 % больных, госпитализированных в сроки после 24 часов с начала заболевания, выявлены деструктивные изменения в ЖП (флегмонозный ОХ — у 88,6 %, гангренозный — у 11,3 % больных. У 64,3 % больных этой группы клинические проявления «запаздывали» от динамики морфологических изменений в стенке ЖП.
Таким образом, внедрение лапароскопической диагностики позволяет объективизировать показания к своевременному выполнению оперативного вмешательства, что способствовало повышению хирургической активности при ОХ с 54,5 % в 1996 до 88,6 % в 2014 году.
Превалирующее количество ЛХЭ (60,8 %) выполнено в день госпитализации, а в сроки до 48 часов прооперировано (94,6 %) пациентов и лишь 5,4 % больных оперированы в сроки 48–72 часов.
Следует отметить, что удельный вес ЛХЭ по мере приобретения опыта ее выполнения сотрудниками отделения эндохирургиии НХЦ под руководством академика М. М. Мамакеева вырос с 11,5 % в 1996 году до 94,5 % в 2014 г. Значительные технические сложности при выполнении ЛХЭ встретились нам у 40,2 % больных ОХ.
К конверсии на ТХЭ прибегали в 162 (%) случаях. Если говорить о мотивах конверсии, то по абсолютным показаниям осуществлен переход на ТХЭ в 80,2 % случаях, а по благоразумию в 18 % случаев.
По благоразумию КЭХ применена из-за невозможности дифференциации анатомических структур, ввиду выраженного воспалительного процесса в области гепатодуоденальной связки, выраженного спаечного процесса в зоне операции, гангрены ЖП в 47 % случаях. Интраоперационные осложнения ЛХЭ, которые возникли у 86 больных, что составляет 6,0 %, представлены в таблице 4.
Таблица 4
Интраоперационные осложнения ЛХЭ убольных ОХ
|
Осложнения |
абс |
% |
|
Кровотечение из пузырной артерии |
16 |
|
|
Кровотечение из ложа ЖП |
25 |
|
|
Желчеистечение из ложа ЖП |
28 |
|
|
Повреждение холедоха |
10 |
|
|
Повреждение воротной вены |
2 |
|
|
Повреждение ЖП |
18 |
|
|
Всего |
86 |
6,0 |
В 20 % случаев остановка кровотечения из пузырной артерии была осуществлена лапароскопическим путем за счет прицельного ее клиппирования.
Приводим клинический пример повреждения магистрального желчного протока:
Больная Абдрахманова К. 53 года. История болезни № 161. Дата поступления 04.01.2003г.
Жалобы при поступлении на боли в правом подреберье, тошноту, рвоту, сухость горечь во рту. Из анамнеза — болеет с 03.01.2003г, когда после приема жирной пищи появились вышеуказанные жалобы.
Общее состояние относительно удовлетворительное, кожные покровы обычной окраски. ЧД — 18 вд.в 1мин; пульс — 90 уд. в мин. АД — 160\100 мм. ст.ст. Язык сухой обложен белым налетом, живот болезненный в правом подреберье, там же мышечное напряжение положительный симптом Ортнера.
Общий анализ крови — Эр — 4,6; гемоглобин — 138; ЦП — 0,9; лейкоциты — 7,5; СОЭ — 28 мм/ч
Общий анализ мочи — белок — 0,033г/л; пл.эп — в большом количестве; лейкоциты — 8–10.
УЗИ — острый калькуллезный холецистит.
06.01.2003г. операция: лапараскопия, лапаратомия, холецистэктомия, холедохохоледохостомия со скрытым дренажем.
Во время операции, при лапараскопическом выделении пузырного протока был перерезан общий желчный проток. Произведена лапаратомия, желчный пузырь удален от шейки. Найдены проксимальный и дистальный концы холедоха, наложен анастамоз конец в конец, со скрытым дренажем.
В послеоперационном периоде у больной было желчеистечение, которое самостоятельно закрылось. Больная выписана с выздоровлением 03.02.2003г. Скрытый дренаж был удален через 1 месяц с помощью фибродуоденоскопа.
Желчеистечение из ложа ЖП в количестве 50–200 мл в сутки имело место у 16 больных. Желчеистечение у них прекратилось самостоятельно на 2–3 сутки. В целом, послеоперационный период проходил без осложнений у 90,7 % больных.
Приводим клинический пример:
Больная Анарбаева З. М. 37 лет. История болезни № 7215. Дата поступления 24.12.2014г. Жалобы при поступлении на боли в правом подреберье, тошноту, рвоту, сухость горечь во рту. Из анамнеза — болеет с 23.12.2014г. когда после приема жирной пищи появились вышеуказанные жалобы.
Общее состояние относительно удовлетворительное, кожные покровы обычной окраски. ЧД — 17 вд.в 1мин; пульс — 94 уд. в мин. АД — 120\80 мм. ст.ст. Язык сухой обложен белым налетом, живот болезненный в правом подреберье, там же мышечное напряжение положительный симптом Ортнера.
Общий анализ крови — Эр — 4,6; гемоглобин — 98; ЦП — 0,8; лейкоциты — 10,9; СОЭ — 26 мм/ч
Общий анализ мочи — белок — 0,033г/л; пл.эп — единицы; лейкоциты 3–4.
УЗИ — острый калькуллезный холецистит, холедох не расширен.
26.12.2014г. операция: лапараскопическая холецистэктомия.
Операция выполнена без особых сложностей, из-за выраженного воспалительного процесса в правом подпеченочном пространстве данная область была задренирована резиновой полоской и микроирригатором. В послеоперационном периоде у больной началось желчеистечение через дренажную рану, которое самостоятельно закрылось на 24 сутки.
Выписана с выздоровлением 30.01.2014г.
Следует отметить, что на протяжении 3–5 суток проводили антибактериальную, детоксикационную и коррегирующую терапию. Антибиотикотерапию проводили на протяжении 2–3, а при осложненном течении заболевания в течение 3–6 суток.
Предпочтение отдавали антибиотикам цефалоспоринового ряда 3–4 поколений (цефобид, клафоран, кефзол, фортум, зинацеф и др.). Причем, 2/3 суточной или суточную дозу указанных антибиотиков вводили внутривенно перед вводным наркозом, последующую — через 6–8 часов после операции.
Возможность ранней двигательной активности (через 10–12 часов после операции) способствовала уменьшению количества послеоперационных осложнений со стороны сердечно-сосудистой системы и органов дыхания, а также раннему восстановлению перистальтики кишечника (1–2 сутки).
Послеоперационные осложнения имели место у 9,2 % больных, среди которых желчеистечение из ложа ЖП обусловили необходимость расширения раны, инфильтраты или абсцессы ложа ЖП и подпеченочного пространства, которые в 2 случаях были ликвидированы путем ревизии и последующего дренирования под наркозом.
Из других осложнений следует упомянуть инфильтрат в месте извлечения ЖП, пневмония. Релапаротомия выполнена лишь 4 больным (%) по поводу поддиафрагмального и подпеченочного абсцессов.
Таким образом, приобретенный нами опыт эндохирургического лечения больных ОХ на первом этапе внедрения ТЭХ при ЖКБ, ХХ и ОХ позволяет утверждать, что формальное выполнение основных положений активно-консервативной терапии в подавляющем большинстве случаев ОХ не оправдано.
Безусловно, приоритетным является выполнение ЛХЭ в первые 48 часов заболевания. Обязательными условиями успешного выполнения лапароскопических оперативных вмешательств при ОХ является наличие достаточного опыта их выполнения, от чего напрямую зависит непосредственные и ближайшие исходы ЛХЭ.
Об этом свидетельствуют результаты второго этапа применения ЛЭХ при ЖКБ, ХХ и ОХ. Как уже отмечалось выше, при выполнении ЛХЭ при ОХ использовали ряд усовершенствованных или разработанных нами технических приемов.
В основной группе мы использовали модифицированную методику ЛХЭ. Сутью ЛХЭ из 3 доступов заключается в следующем:
во-первых, мы устанавливаем 12 или 10-мм троакар на 1 см ниже пупочного кольца по средней линии — для введения телескопа;
во-вторых, после проведения обзорной лапароскопии устанавливаем второй 10-мм-вый троакар по средней линии, отступя от мечевидного отростка одну четверть расстояния между ним и пупком для выполнения всех этапов холецистэктомии;
в-третьих, устанавливаем третий порт 6-мм-вый по правой переднеаксилярной линии ниже реберной дуги на 2–4 см.
Через этот лапаропорт проводится эндограспер, которым производится тракция шейки и Гартмановского кармана ЖП, а на этапе выделения ЖП из ложа с помощью ротации и тракции без фиксации за дно ЖП. Это очень важный момент ЛХЭ.
Выделение и препаровку ЖП производим эндодиссектором с коагуляцией, проведенным через второй троакар. Тракцию ЖП за дно проводим эндограспером, проведенным через 3-ий лапаропорт.
При выраженном спаечном процессе в подпеченочном пространстве разделение спаек и выделение ЖП можно выполнить так же используя только два инструмента. Разделение спаек производим и коагуляционным крючком.
В нашей практике идентификацию пузырного протока с помощью эндодиссектора производим через второй троакар (эпигастральный), используя переходник с 10 мм на 5 мм. Эндодиссектором производим дальнейшую препаровку и выделение элементов треугольника Кало, подготавливаем к клипированию пузырный проток и артерию.
Затем убираем переходник из второго троакара и производим клиппирование пузырного протока и артерии. С помощью электрокоагуляционного крючка выделяем ЖП из ложа. ЖП захватывается эндограспером через 3-й троакар за шейку или Гартмановский карман и, «закручивая» кверху-кнаружи, производится его постоянная тракция.
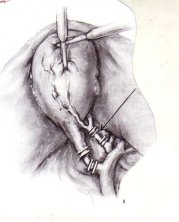
Рис. 1. Схема хорошо визуализированного наложения клипов на пузырный проток и пузырную артерию (Больной Т., 48 лет)
После отделения ЖП через 2-й троакар вводится эндограспер и ЖП извлекается из брюшной полости через 10 мм (эпигастральный) троакар. При наличии в просвете крупных (более 10 мм) конкрементов прибегаем либо к расширению раны апоневроза, либо к фрагментации конкрементов в просвете пузыря.
Учитывая значительную толщину стенки ЖП при ОХ за счет ее инфильтрации, адекватный захват ЖП и обеспечение тракции осуществляли только 10 мм зажимом, который вводили через 11 мм троакар по переднеаксилярной линии.
В последующем его использовали и для введения дренажной трубки толщиной 7–8 мм, что обеспечивало адекватную эвакуацию содержимого брюшной полости, обязательно проводили пункцию и эвакуацию содержимого с последующей герметизацией с помощью зажима или эндопетли.
При наличии диффузной кровоточивости тканей гемостаз осуществляли не после выделения ЖП, а в ходе выполнения каждого из этапов операции, преимущественно методом гидрокоагуляции.
Инфильтрированный ЖП удаляли, как правило, в целофановом или пластиковом мешке через троакар в эпигастральной области, что позволило во всех случаях избежать развития послеоперационных грыж.
При напряженном ЖП, особенно в момент извлечения его из брюшной полости, для уменьшения его объема производим пункцию, эвакуируем желчь, затем удаляем ЖП из брюшной полости под визуальным контролем. Производим ревизию ложа ЖП, при необходимости санацию подпеченочного пространства, выполняем десуфляцию.
Длительность модифицированной операции не превышала времени традиционной ЛХЭ. Необходимости конверсий не возникло. В 26 случаях интраоперационных осложнений пришлось воспользоваться четвертым лапаропортом.
12 раз это дополнение состоялось при повреждении пузырной артерии и 4-ый троакар был установлен для фиксации и клиппирования культи пузырной артерии.
У 16 пациентов возникло кровотечение из ложа ЖП, последнее остановлено лапароскопически путем наложения пластины «Тахокомб», но для удобства работы был установлен 4 лапаропорт.
При интраоперационной перфорации стенки ЖП отверстие закрывали путем наложения на него эндограспера, основная функциональная нагрузка которого заключалась в тракции ЖП. Санацию проводили раствором фурацилина аквапуратором из 2-го лапаропорта. Страховочный дренаж установлен к ложу ЖП через 3-ий лапаропорт под визуальным контролем.
Случаев повреждения холедоха среди оперированных нами больных не было, чему способствовало скрупулезное, тщательное выполнение всех этапов ЛХЭ с учетом анатомических вариантов внепеченочных желчных путей, ЖП, сосудистой системы в зоне операции, характера патологического процесса и других факторов. Послеоперационный период при модификации техники ЛХЭ у всех больных протекал без осложнений.
Таким образом, накопление опыта выполнения ЛХЭ у больных ОХ позволяет успешно выполнять модифицированную ЛХЭ. ЛХЭ из 3 доступов не сужает технические возможности оператора, в том числе и при интраоперационных осложнениях, не ограничивает долженствующий объём операции даже при спаечном процессе, усиливает эффект малоинвазивности вмешательства, является перспективной оперативной технологией у больных ОХ.
Заключение.
Приобретенный нами опыт хирургического лечения больных ОХ с максимально ранним выполнением лапароскопической диагностики больным позволяет своевременно оценить хирургическую ситуацию и выполнить адекватное оперативное вмешательство в первые 12–48 часов заболевания.
Обязательными условиями успешного выполнения лапароскопических и эндоскопических оперативных вмешательств при ОХ является наличие достаточного опыта их выполнения. ЛХЭ имеет свои ограничения и пределы разрешающей способности, учитывать которых необходимо хирургу любого профессионального опыта.
Внедрение лапароскопических технологий способствует существенному увеличению удельного веса ОХ, которым выполнены оперативные вмешательства, что является важнейшим условием улучшения ближайших и отдаленных результатов оперативных вмешательств. Между тем, существуют риск применения этого метода при ряде обстоятельств, которых следует учитывать в своей практике.
Существуют ряд нерешенных проблем, касающихся конверсии ЛХЭ в ТХЭ: показания, переход по благоразумию, сроки и тактика послеоперационного ведения больных. Для их разрешения необходим анализ причин конверсии с оценкой прогностической значимости ряда признаков.







