На примере адсорбции изоамилового спирта из раствора исследована адсорбционная способность гранулированного силикагеля, гранулированного активного угля и порошка-наполнителя фильтра «Аквафор». Экспериментально полученные изотермы поверхностного натяжения и изотермы адсорбции показали, что более высокой адсорбционной способностью обладает порошок «Аквафор». Величина адсорбции на данном порошке была в несколько раз выше, чем на угле и силикагеле.
Ключевые слова: поверхностное натяжение, адсорбент, адсорбция, поверхностно-активное вещество (ПАВ)
Адсорбция из раствора на твердых адсорбентах имеет большое практическое значение и широко применяется для очистки воды и воздуха, в различных процессах для разделения газовых и жидких смесей, в медицинской практике для очистки организма от токсичных веществ, в гетерогенном катализе и т. д.
Адсорбция из растворов, по сравнению с газовой адсорбцией, — значительно более сложное явление. Во-первых, скорость и величина адсорбции зависят от природы и концентрации растворенного вещества (адсорбтива) и природы растворителя. Растворенное вещество может адсорбироваться на поверхности от адсорбента, только вытесняя молекулы растворителя. Во-вторых, адсорбция зависит от химического состава и удельной поверхности самого адсорбента. В качестве адсорбентов используются активированные угли, силикагели, цеолиты др.
Для характеристики адсорбента используют изотерму адсорбции — зависимость адсорбции (Г, моль/см2) от концентрации растворенного вещества (С, моль/л). В случае твердых адсорбентов, если не известна точная площадь поверхности, адсорбцию рассчитывают как отношение количества адсорбированного вещества (x) к массе адсорбента (m): Г=x/m (моль/г) [1]. Экспериментально величину адсорбции Г=x/m находят по разности между начальной концентрацией раствора (С0) и концентрацией, установившейся при достижении адсорбционного равновесия (Сравн) [1].
Целью данной работы было исследовать и сравнить адсорбционную способность некоторых твердых адсорбентов различной природы на примере адсорбции ПАВ (поверхностно-активного вещества) из раствора.
Материалы иметоды
В качестве твердых адсорбентов применялись: 1) гранулированный силикагель; 2) гранулированный активный уголь; 3) порошок-наполнитель бытового очистителя для воды марки «Аквафор».
Для оценки адсорбционной способности в качестве адсорбтива применяли изоамиловый спирт (3-метил-бутанол-1) — (CH3)2CHCH2CH2OH — неионогенное ПАВ с плотностью 0,81 г/см3. Изоамиловый спирт ядовит, является основным компонентом сивушного масла. Готовили растворы (с использованием дистиллированной воды) концентрацией от 0,004 до 0,2 моль/л.
Поверхностное натяжение раствора измеряли методом максимального давления в пузырьке воздуха с помощью прибора Ребиндера [2]. Величину адсорбции на поверхности жидкость/твердый адсорбент — Г=x/m (моль/г) — рассчитывали по уравнению:
![]()
где С0 и Сравн — начальная и равновесная концентрация спирта в растворе, соответственно; V — объем раствора (25 мл); m — масса твердого адсорбента (1 г).
Размер частиц адсорбентов определяли методом оптической микроскопии с применением видеокамеры Levenhuk C510.
Результаты
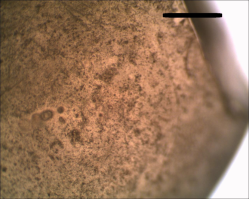
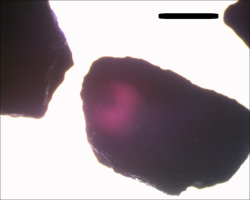
На примере адсорбции ПАВ (изоамилового спирта) из раствора исследована адсорбционная способность гранулированного силикагеля, гранулированного активного угля и порошка «Аквафор». На рис. 1 показаны микрофотографии гранул этих адсорбентов. Размер и форма гранул: 1) силикагель — сферические гранулы диаметром 3–6 мм; 2) уголь — гранулы длиной 1–2 мм и толщиной около 1 мм; 3) порошок «Аквафор» — сферические ионообменные гранулы диаметром 160–330 мкм и угольные частицы размером 300–600 мкм.
(а) (б)

(в)
Рис. 1. Оптические микрофотографии частиц адсорбентов: а) силикагель (поверхность гранулы); б) уголь; в) порошок «Аквафор». Шкала — 500 мкм.
Силикагель — представляет собой пористые гидрофильные гранулы высушенного геля поликремниевых кислот ![]() . Активный уголь — пористый углерод, гидрофобный органический адсорбент, получаемый из древесного или каменного угля. Порошок «Аквафор» содержит ионообменное волокно «Аквален» и активированный кокосовый уголь [3]. Поскольку все адсорбенты пористые, то размер гранул не должен заметно влиять на их адсорбционные свойства.
. Активный уголь — пористый углерод, гидрофобный органический адсорбент, получаемый из древесного или каменного угля. Порошок «Аквафор» содержит ионообменное волокно «Аквален» и активированный кокосовый уголь [3]. Поскольку все адсорбенты пористые, то размер гранул не должен заметно влиять на их адсорбционные свойства.
На рис. 2 и 3 представлены экспериментально полученные изотермы поверхностного натяжения σ(С0) и изотермы адсорбции Г(Сравн), наглядно характеризующие адсорбционную способность исследованных адсорбентов. Чем больше поверхностное натяжение раствора после контакта с адсорбентом (рис. 2), и чем больше величина адсорбции при данной концентрации (рис. 3), тем выше адсорбционная способность вещества и, следовательно, тем эффективнее очистка воды с помощью данного адсорбента.
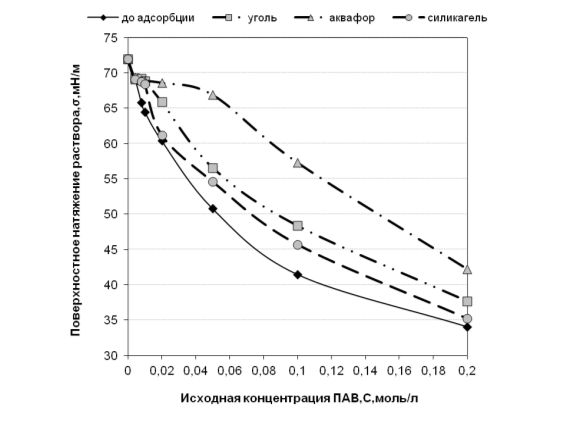
Рис. 2. Изотермы поверхностного натяжения σ(С0) раствора изоамилового спирта до адсорбции (сплошная линия) и после адсорбции на твердых адсорбентах
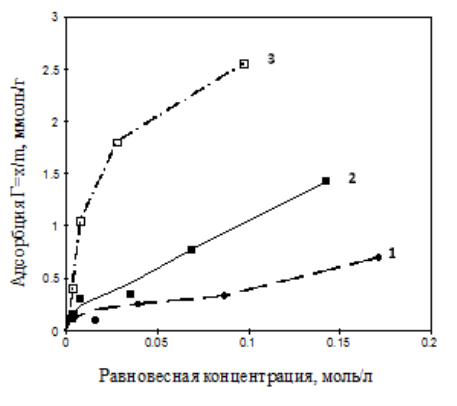
Рис. 3. Изотермы адсорбции Г(Сравн) изоамилового спирта на твердых адсорбентах: 1 — силикагель; 2 — уголь; 3 — порошок «Аквафор»
Как видно из кривых σ(С0) и Г(Сравн), более высокой адсорбционной способностью обладает порошок «Аквафор». Так, например, при равновесной концентрации изоамилового спирта 0,1 моль/л адсорбция на наполнителе «Аквафор», содержащем в основной массе угольные частицы (см. рис. 1), была примерно в 2,5 раза больше, чем на угле с гранулами миллиметрового размера, и примерно в 8 раз больше, чем адсорбция на силикагеле. Как уже было отмечено, все адсорбенты имели пористую структуру, поэтому большая эффективность «Аквафора» объясняется не размером гранул, а, возможно, более высокой удельной поверхностью и дегазацией поверхности.
Сравнительно меньшая адсорбционная активность силикагеля связана с гидрофильностью его поверхности в отличие от гидрофобных углей. Известно, что, чем лучше смачивание адсорбента растворителем, тем хуже адсорбция растворенного вещества на его поверхности [1].
Интересно, что в серии наших экспериментов по адсорбции красящего вещества чернил [4] лучшую адсорбционную активность проявил диатомит, не смотря на его гидрофильные свойства (состоит из оксидов кремния, алюминия, железа, кальция и магния). В этой же серии экспериментов адсорбция чернил на активированном угле мало отличалась от адсорбции на силикагеле и цеолите [4]. Адсорбирующимся веществом в этом случае был краситель, в состав которого входит метиловый фиолетовый, имеющий более разветвленную молекулярную структуру (три бензольных кольца) в отличие от изоамилового спирта. Вероятно, лучшая адсорбция красящего вещества чернил объясняется его более развитым углеводородным скелетом.
Заключение
Адсорбция на порошке «Аквафор» была в несколько раз выше, чем на активированном угле и силикагеле.
Литература:
- Кругляков П. М., Хаскова Т. Н. Физическая и коллоидная химия: учеб. пособие. М.: Высшая школа, 2010.
- Кругляков П. М., Нуштаева А. В., Вилкова Н. Г., Кошева Н. В. Физическая и коллоидная химия. Практикум: учеб. пособие. С.-Пб.: Лань, 2013.
- Аквален // Аквафор / [Электронный ресурс]. — Режим доступа: http://www.aquaphor.ru/aqualen (дата обращения 24.06.2016 г).
- Жанабергенова Д. Р., Мещанинова Ю. О. Определение поглотительной способности наиболее известных адсорбентов / Молодой учёный, 2015, № 11 (91), с. 492–497.







