Исследовано влияние различных концентраций инсулина (10–2–10–9 г/мл) на метаболическую активность нейтрофилов крови человека с помощью хемилюминесцентного метода. Выявлено изменение уровня перекисного окисления липидов (ПОЛ) и фагоцитарной активности нейтрофилов. Показана возможность модуляции радикальной активности нейтрофилов через рецепторы к инсулину с помощью температур.
Ключевые слова: нейтрофилы, инсулин
При коррекции гипергликемии в комплексной терапии генерализованных воспалительных состояний большое внимание уделяется иммунорегулирующему действию инсулина. Имеются обширные сведения о локализации, химической природе, обмене и функциональной активности рецепторов к инсулину в норме и при патологии [1–4]. Строение инсулинового рецептора, способность различных инсулинов связываться с рецепторами и вызывать биологические реакции, практически идентичны в клетках всех типов и всех видов. Рецептор к инсулину с высокой специфичностью распознает в молекуле места связывания инсулина, осуществляет комплексирование с ним и опосредует передачу соответствующего сигнала, направленного на активацию внутриклеточных обменных процессов. Известно, что при активации многокомпонентного энзима плазматических мембран нейтрофилов — НАДФН-оксидазы в клетках повышается содержание реактивных кислородных метаболитов, влияющих на степень фосфорилирования многих клеточных ферментов и, следовательно, изменяющих их активность [5, 6]. НАДФН-оксидаза нейтрофилов играет важную роль в фагоцитарных реакциях, защищая организм от патогенов и являясь одним из факторов, запускающих воспалительный ответ. Снижение активности НАДФ-зависимой оксидазы является одним из механизмов фагоцитарной недостаточности клеток. В настоящее время ведется поиск новых неагрессивных способов восстановления данной функции. С учетом выше сказанного целью настоящей работы явилось определение влияния температурных воздействий на активность инсулиновых рецепторов нейтрофилов по изменению их радикальной активности.
Материалы иметоды исследования
В работе использованы лейкоциты периферической крови доноров-добровольцев (n=17), инсулин растворимый человеческий генно-инженерный (препарат инсулина короткого действия «Актрапид НМ», Ново Нордиск А/С, Дания) в различных концентрациях (10–2–10–14 г/мл). Для приготовления разведения раствора инсулина применен раствор Хенкса стерильный (ООО «БиолоТ», СПб). Исследования выполнены в осенне-зимний период. В связи с тем, что среди клеток крови основным продуцентом активных форм кислорода, обладающих бактерицидным действием, являются нейтрофилы, при оценке хемилюминесценции венозной или капиллярной крови интенсивностью свечения моноцитов и лимфоцитов пренебрегают [7].
В качестве температурного воздействия применены следующие температуры: +45°С, +2°С и -2°С. В опытах с температурами +45°С и +2°С кровь разливали по 2 мл в микропробирки и выдерживали при указанных температурах в течение 30 мин, используя для этих целей соответственно термостат для микропробирок «Гном» и бытовой электрический холодильник «Саратов»-1615М.
В опытах с температурой -2°С кровь в пластикатной пробирке в объеме 5 мл помещали в электрический морозильник «Derby» (Дания) на -20°С. С помощью цифрового дистантного термометра «Checktemp 1» (Румыния) контролировали температуру охлаждаемой клеточной взвеси. Средняя скорость снижения температуры составляла 2.3°С/мин. Отмечалось плавное снижение температуры без выброса кристаллизационного тепла с сохранением вязкого состояния биообъекта. Общее время охлаждения составляло 9–10 мин. Сохранность клеток, подвергнутых охлаждению до -2°С, оценивали с помощью метода световой микроскопии (Nikon H550S, Япония) в пробах с 1.0 % раствором суправитального красителя эозина, считая признаком повреждения клеточной мембраны диффузное окрашивание цитоплазмы в розовый цвет. Необходимо отметить, что данное температурное охлаждение во всех случаях не вызывало статистически значимой гибели клеток.
Влияние инсулина различных концентраций на интенсивность ПОЛ и активность антиоксидантных систем нейтрофилов оценивали с помощью метода индуцированной (перекисью водорода с сульфатом железа) хемилюминесценции на биохемилюминометре БХЛ-07 (ЦНИЛ НГМА; «ИМБИО» Нижний Новгород). В измерительную кювету прибора вносили 0.1 мл крови с инсулином в соответствующей концентрации и 0.4 мл фосфатного буфера (рН=7.5), добавляли 0.4 мл 0.01 мМ раствора сульфата железа (ОАО «Спектр-Хим» г. Москва) и помещали в измерительную кювету. После чего в нее быстро вносили 0.2 мл 2 % раствора перекиси водорода (ЗАО «СП Химпром» г. Самара) и регистрировали сигнал в течение 30 сек. Оценивали следующие параметры: Imax (мВ) — максимальную интенсивность быстрой вспышки, отражающей потенциальную способность биологического объекта к свободно радикальному окислению; S (мВ×сек) — светосумму за 30 сек, отражающую содержание радикалов RO2; tg(-2α) — тангенс угла наклона кривой оси времени (характеризует максимальную крутизну спада кривой, со знаком «-»), чем выше значение показателя tg(-2α), тем выше активность ферментативных систем клеток, регулирующих содержание гидроперекисей.
При оценке влияния инсулина различных концентраций на степень активности НАДФН-оксидазы нейтрофилов с помощью БХЛ-07 к 0.1 мл смеси крови с инсулина в соответствующей концентрации добавляли 0.05 мл раствора латекса диаметром 0.08 мкм («Sigma-Aldrich», Германия). Затем в измерительную кювету вносили 0.05 мл подготовленной пробы, добавляли 0.95 мл раствора Хенкса и 0.2 мл рабочего раствора люминола. Кювету помещали в измерительную камеру, включали режим перемешивания и термостатирования (+37°С). Измерение проводили в течение 30 мин. При автоматическом вычете уровня шума регистрировали следующие параметры: Imax (мВ) — максимальное значение интенсивности хемилюминесценции; S (мВ×сек) — светосумму за 30 мин, определяемую как площадь под кривой свечения пробы.
При статистической обработке данных вычисляли среднее арифметическое значение ± среднее квадратичное отклонение (M±δ). Для выявления статистической значимости различий (p<0,05) между группами применяли непараметрический критерий Вилкоксона [8] с использованием компьютерной программы для медико-биологической статистики «BIOSTAT».
Результаты исследования
Установлено (табл. 1), что инсулин в высоких концентрациях, т. е. 10–2–10–4 г/мл вызывает ингибирование процессов ПОЛ у нейтрофилов, при этом снижается и активность антиоксидантных систем клеток, ответственных за утилизацию гидроперекисей. В концентрации из диапазона 10–5–10–14 г/мл инсулин значимого изменения в интенсивности указанных выше процессов не вызывает.
Таблица 1
Влияние различных концентраций инсулина на интенсивность процессов ПОЛ иактивность антиоксидантых систем нейтрофилов периферической крови практически здоровых доноров-добровольцев по показателям хемилюминограмм (n=12, M±δ).
|
Серия |
Показатели хемилюминограммы |
||
|
Iмах (мВ) |
S (мВ×с) |
tg(-2α) |
|
|
Нейтрофилы |
170 ± 18.5 |
1270 ± 180.4 |
33 ± 6.3 |
|
с инсулином 10–2 г/мл |
106 ± 5.5* |
862 ± 50.9* |
16 ± 7.0* |
|
с инсулином 10–3 г/мл |
120 ± 14.4* |
896 ± 158.2* |
24 ± 7.7* |
|
с инсулином 10–4 г/мл |
156 ± 16.4 |
1054 ± 84.2* |
35 ± 3.9 |
|
с инсулином 10–5 г/мл |
171 ± 12.5 |
1175 ± 44.4 |
36 ± 4.6 |
|
с инсулином 10–6 г/мл |
165 ± 8.4 |
1185 ± 38.3 |
35 ± 3.7 |
|
с инсулином 10–7 г/мл |
159 ± 9.9 |
1272 ± 147.6 |
32 ± 2.5 |
|
с инсулином 10–8 г/мл |
168 ± 16.0 |
1221 ± 120.8 |
35 ± 5.9 |
|
с инсулином 10–9 г/мл |
173 ± 26.0 |
1273 ± 240.4 |
37 ± 6.6 |
|
Примечания: * — p<0.05 от значения нейтрофилов; в связи с отсутствием значимого эффекта в таблице не приведены данные серий с инсулином в концентрации 10–10–10–14 г/мл. |
|||
Показано, что в присутствии препарата инсулина «Актрапид НМ» в концентрации 10–7 г/мл радикальный ответ нейтрофилов на наличие в среде чужеродного объекта — частиц латекса был неравнозначным: в тех случаях, когда исходный уровень радикальной активности клеток был низким, инсулин его повышал, при высоком исходном уровне — снижал (рис. 1). Таким образом, инсулин выступает в роли модулятора активности нейтрофилов. Обращает на себя внимание, тот факт, что охлаждение клеток до +2°С оказывает действие подобное инсулину. Вероятно, в активации или угнетении радикального ответа нейтрофила инсулином или гипотермией задействован единый механизм, связанный с изменением активности многокомпонентного энзима плазматических мембран нейтрофилов — НАДФН-оксидазы. Известно, что респираторный взрыв регулируется многими рецепторными и нерецепторными реакциями, которые завершаются конформационными изменениями компонентов НАДФН-оксидазы и их готовностью вступать во взаимодействие друг с другом [9]. В условиях нормы энзиматическая активность НАДФ-Н оксидазы ограничена в пространстве фагосомой и во времени аутодеактивацией [10]. При стимуляции нейтрофила фактором корпускулярной или растворимой природы, действующим через рецепторы или по рецептор-независимому механизму происходит быстрая самосборка энзима и наработка активированных форм кислорода. Следует отметить, что инсулин значимо повышает радикальный ответ у нейтрофилов после их экспозиции при +2°С в том случае, когда исходный уровень активности НАДФН-оксидазы был относительно низким (рис. 1). Возможно, температурное воздействие +2°С, как адекватный стресс-фактор способствует увеличению количества рецепторов к инсулину на мембранах «слабых» нейтрофилов.
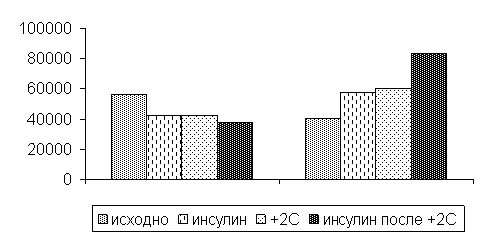
Рис. 1. Влияние инсулина (10–7 г/мл) и гипотермии (30 мин при +2°С) на активность НАДФН-оксидазы нейтрофилов по показателю медианы светосуммы (S)
Показано, что гипертермическое воздействие (+45°С, 30 мин, in vitro) полностью блокирует способность НАДФН-оксидазы нейтрофилов продуцировать кислородные метаболиты. Биологическое действие температур выше +42°С — подавлять активность ферментов — используется в программе многокомпонентного лечения в современной клинической онкологии [11]. Установлено, что инсулин (10–7 г/мл) не изменяет радикальную активность клеток, подвергнутых гипертермии.
Установлено, что охлаждение нейтрофилов до -2°С снижает способность НАДФН-оксидазы генерировать активированные формы кислорода, что может быть связано с нарушением самосборки НАДФН-оксидазы из мембранных и цитозольных компонентов при охлаждении. Известно [12], что при 0°С и ниже — происходит снижение гидрофобных взаимодействий структурных компонентов мембран и их перестройка, которая вызывает угнетение функций ферментов, возможно в мембранах лейкоцитов данный процесс имеет место при -2°С. В присутствии инсулина (10–7 г/мл) радикальный ответ нейтрофилов, подвергнутых охлаждению до -2°С на наличие в среде чужеродного объекта — частиц латекса был неравнозначным: в тех случаях когда уровень радикальной активности у нативных клеток был относительно высоким, инсулин способствовал его повышению, а в тех случаях когда исходный уровень был низким — значимо ингибировал его (рис. 2). Следовательно температурное воздействие -2°С, как агрессивный стресс-фактор способствует снижению количества активных рецепторов к инсулину на мембранах «слабых» нейтрофилов.

Рис. 2. Влияние инсулина (10–7 г/мл) и гипотермии (охлаждение до -2°С) на активность НАДФН-оксидазы нейтрофилов по показателю светосуммы (S)
Таким образом, полученные данные свидетельствуют о том, что инсулин также как и температурное воздействие может выступать в роли модулятора радикальной активности нейтрофилов крови человека. Возможность температурной модуляции активности НАДФН-оксидазы нейтрофилов через рецепторы к инсулину может стать новым путем управления эффекторными механизмами иммунитета.
Выводы
- Инсулин (10–7 г/мл) значимо повышает радикальный ответ у нейтрофилов периферической крови человека на наличие в среде чужеродного объекта — частиц латекса после гипотермического воздействия (+2°С, 30 мин) в том случае, когда исходный уровень активности НАДФН-оксидазы клеток снижен.
- Инсулин (10–7 г/мл) не изменяет радикальную активность нейтрофилов, подвергнутых гипертермическому воздействию (+45°С, 30 мин), которое полностью блокирует способность НАДФН-оксидазы клеток продуцировать кислородные метаболиты.
- Инсулин (10–7 г/мл) значимо снижает радикальный ответ у нейтрофилов периферической крови человека на наличие в среде чужеродного объекта — частиц латекса после гипотермического воздействия (охлаждение до +2°С) в том случае, когда исходный уровень активности НАДФН-оксидазы клеток снижен.
Литература:
- Бутакова С. С., Ноздрачев А. Д. Физиологические механизмы секреции кальцитонина при инсулиновой гипогликемии // Вестн. С-Петерб. ун-та. Сер. 3.. — 2010. — № 2. — С. 100–106.
- Петракова О. В., Сыманович О. Ю., Хватова Л. А., Гурманчук И. Е. Особенности иммунологического действия инсулина и глюкозы на нейтрофилы и лимфоциты человека in vitro // Мат-лы II междун. конф. «Молодой ученый. Новые задачи современной медицины».. — Санк-Петербург: Реноме, 2013. — С. 27–29.
- John G. Menting, Jonathan Whittaker, Mai B. Margetts, Linda J. Whittaker, Geoffrey K.-W. Kong, Brian J. Smith, Christopher J. Watson, Lenka Žáková, Emília Kletvíková, Jiří Jiráček, Shu Jin Chan, Donald F. Steiner, Guy G. Dodson, Andrzej M. Brzozowski, Michael A. Weiss, Colin W. Ward and Michael C. Lawrence. How insulin engages its primary binding site on the insulin receptor // Nature. — 2013. — № 7431. — С. 241–245.
- Shaodong Guo. Insulin Signaling, Resistance, and the Metabolic Syndrome: Insights from Mouse Models to Disease Mechanisms // J. Endocrinol.. — 2014. — № 2. — С. 1–23.
- Rhee S. G. Cell signaling. H2O2, a necessary evil for cell signaling // Science. — 2006. — № 312. — С. 1882–1883.
- Берлов М. Н., Кораблева Е. С., Филимонов В. Б., Кокряков В. Н. Исследование антимикробной активности миелопероксидазы и лактоферрина // Вестн. С.-Петерб. ун-та. Сер. 3. — 2009. — № 1. — С. 83–89.
- Панасенко Л. М., Краснова Е. И., Ефремов А. В. Клиническое значение хемилюминесцентного ответа лейкоцитов крови при коклюше // Бюллетень СО РАМН. — 2005. — № 4. — С. 44–47.
- Гланц С. Медико–биологическая статистика. — М.: Практика, 1998. — 459 с.
- Маянский А. Н. НАДФН-оксидаза нейтрофилов: активация и регуляция // Цитокины и воспаление. — 2007. — № 3. — С. 3–13.
- Меньщикова Е. Б., Ланкин В. З., Зенков Н. К., Бондарь И. А., Круговых Н. Ф., Труфакин В. А. Окислительный стресс. Прооксиданты и антиоксиданты. — М.: Слово, 2006. — 556 с.
- Кисличко А. Г., Кисличко С. А., Поздеев Н. М. Лечебный эффект гипертермии в комбинированном лечении при немелкоклеточном раке легкого // Вятский медицинский вестник. — 2012. — № 1. — С. 54–59.
- Белоус А. М., Грищенко В. И. Криобиология. — Киев: Наукова думка, 1994. — 432 с.







