This article presents the results of a systematic analysis accented access technology, audit, operational administration, sanitation and drainage of the abdominal cavity sanation at relaparotomy (SRL) in patients with postoperative peritonitis (PP) was caused by complications of acute pancreatitis (PLO). The analysis included the results of the target intervyurovaniya surgeons involved in the SRL. When rondomizatsii by the presence of multiple organ dysfunction (MODS) were allocated two clinical groups: group A, which included patients without the OPA; Group B, which included patients with MODS.
Keywords: Improved sanitation relaparotomy, postoperative peritonitis, acute pancreatitis, multiorgan failure, rondomizatsiya.
Целью исследования были изучение и анализ результатов лечения больных с осложненным острым панкреатитом и выработка оптимальных показаний к санационной релапаротомии.
Материал и методы исследования. 7 из 8 больных с осложненным острым панкреатитом (ООП) (87 %) подвергнуты санационной релапаротомии (СРЛ) в сроки <72 часов с момента первичной лапаротомии. 62 % оперированных больных были мужского пола.
При рандомизации по наличию полиорганной недостаточности (ПОН) нами выделены две клинические группы (А,Б): группа А, в которую вошли больные без ПОН (n-2); группа Б, в которую вошли больные с ПОН (n-6). У 6 из 8 больных (75 %) имело место ПОН.
У больных обеих групп имеет место умеренная тахикардия и тахипноэ После СРЛ у больных группы Б частота дыхания соответствовал исходному своему значению (р<0,05), а у больных группы А незначительно уменьшалась (р<0,05).
В недельный срок после СРЛ у больных обеих групп суточный диурез был умеренно повышенной, а удельный вес сниженной (р<0,05 и р<0,05). До и после СРЛ у больных обеих групп сохраняется гипохромная анемия, а также высокая СОЭ и лейкоцитоз. Явствует и нейтрофильный сдвиг крови, а также высокий лейкоцитарный индекс интоксикации (ЛИИ) (в среднем 4,30,2 расч.ед., р<0,05) (табл.1).
Таблица 1
Клинико-лабораторные параметры (М±m) в группах А и Б до и после СРЛ (6–7-е сутки)
|
Параметры |
До СРЛ |
Группы |
|
|
А |
Б |
||
|
ЧД, в мин. |
34±2,3 |
33±3,2 |
34±5,5 |
|
ЧСС, в мин. |
120±10,2 |
100±12,2 |
110±10,0 |
|
АД, мм.рт.ст. |
85–95/40–50 |
110–125/60–70 |
95–100/80–85 |
|
Сознание |
Заторможен |
Заторможенное |
Заторможенное |
|
Перистальтика |
отсутствует |
отсутствует |
отсутствует |
|
Температура тела |
Гипертермия |
Субфебрильная |
Субфебрильная |
|
Сут.диурез, мл/ч. |
1600100,0 |
1520±110,3 |
1520±120,0 |
|
Уд.вес мочи |
1015100,5 |
1015±100,6 |
1025±100,2 |
|
Эр. х1012/л |
3,30,3 |
3,7±0,3 |
3,9±0,4 |
|
Hb,г/л |
53,26,3 |
54,2±8,4 |
48,4±8,3 |
|
ЦП,ед. |
0,60,02 |
0,6±0,01 |
0,7±0,02 |
|
СОЭ,мм/ч. |
48,26,2 |
44,4±2,5 |
46,1±3,2 |
|
Лейк. х109/л |
17,21,2 |
12,2±1,3 |
16,1±2,3 |
|
Пал., % |
10,71,1 |
10,3±1,4 |
11,3±2,8 |
|
Сегм., % |
70,64,3 |
71,2±6,3 |
66,4±4,1 |
|
Лимф., % |
12,22,2 |
14,2±2,5 |
15,3±2,4 |
|
Мон., % |
3,20,2 |
4,3±1,3 |
4,1±1,0 |
|
Эозин., % |
1,20,9 |
2,1±0,5 |
2,2±0,3 |
|
ЛИИ, расч.ед. |
6,50,3 |
4,20,1 |
4,50,3 |
Примечание: — достоверно в сравнении с исходным; — достоверно в сравнении подгрупп А и Б.
После СРЛ содержание билирубина в крови, его фракций оставался повышенным (р<0,05). У больных обеих групп активность АСТ умеренно снижается, а активность АЛТ находится на уровне исходных цифр (табл.2).
Таблица 2
Биохимические параметры (М±m) в группах А и Б до и после СРЛ (6–7-е сутки)
|
Показатели |
До СРЛ |
Группы |
|
|
А |
Б |
||
|
Бил.(общ.), мкмоль/л |
36,2±3,1 |
34,3±10,3 |
35,1±2,4 |
|
Бил.(пр.), мкмоль/л |
12,2±2,2 |
10,4±1,2 |
12,5±1,0 |
|
Бил.(непр.), мкмоль/л |
24,3±2,5 |
24,2±6,7 |
22,2±3,1 |
|
АСТ, ммоль/л |
0,8±0,01 |
0,5±0,01 |
0,5±0,01 |
|
АЛТ, ммоль/л |
2,3±0,2 |
2,1±0,2 |
2,3±0,2 |
|
Белок (общ.),г/л |
48,4±2,1 |
49,6±6,0 |
45,1±4,2, |
|
Альбум., % |
28,6±9,3 |
28,2±11,1 |
28,3±7,1 |
|
γ-глобулин, % |
6,7±1,0 |
6,2±1,8 |
6,6±1,1 |
|
Тимоловая проба,ед. |
9,4±1,2 |
8,3±1,1 |
9,1±1,0 |
|
Сулемовая проба,ед. |
2,7±0,2 |
2,7±0,3 |
3,1±0,2 |
|
Амилаза,г/час.л. |
93,2±9,2 |
88,6±4,3 |
108,2±11,2, |
|
Ост.N., ммоль/л |
36,4±4,2 |
32,2±3,2 |
36,2±3,2 |
|
Мочевина, ммоль/л |
10,1±2,7 |
11,6±1,2 |
12,5±2,5 |
|
Креатинин, ммоль/л |
185,1±12,6 |
180,0±10,2 |
196,2±18,3 |
|
Na, ммоль/л |
141,2±1,2 |
145,1±1,5 |
142,2±1,1 |
|
К, ммоль/л |
3,9±0,1 |
3,3±0,2 |
3,3±0,1 |
Примечание: — достоверно в сравнении с исходной; — достоверно в сравнении подгрупп А и Б.
Общий белок незначительно снижается у больных группы Б. После СРЛ показатель тимоловой пробы снижается, а сулемовой возрастает лишь у больных группы Б (р<0,05). В этой группе больных возрастает и содержание амилазы (р<0,05).
После СРЛ остаточный азот, мочевина и креатинин крови имеют тенденцию к уменьшению лишь у больных группы А (р<0,05). У больных обеих групп после СРЛ сохраняется гипернатриемия и склонность к гипокалиемии (р<0,05 и р<0,05).
Результаты и обсуждение. Таким образом, у больных шансы на неблагополучный исход в 2,6 раза превышает таковую благоприятного исхода. Практически, исход не зависит от профессиональной квалификации хирурга (ПКХ), а целиком зависит от степени выраженности ПОН.
После СРЛ погиб 1 больной группы Б, что составляет 16,7 %. В группе А также погиб 1 больной, что составляет 50 %. Таким образом, летальность в группах сравнения наблюдалась лишь у больных с ПОН. Летальность в подгруппе Б превышает летальность в аналогичной подгруппе больных на 33,3 %.
Результаты систематического анализа акцентируемых технологий доступа, ревизии, оперативного приема, санации и дренирования брюшной полости при СРЛ у больных послеоперационный перитонит (ПП) причиной которого была ООП. Анализ включал и результаты целевого интервьюирования хирургов, привлеченных к СРЛ.
Как утверждают хирурги с опытом релапротомий (РЛ), здравый смысл диктует, что при при вынужденной СРЛ у больных после операции на поджелудочной железе, предпринятой по поводу ООП, прямой доступ к патологическому очагу предпочтителен.
Чаще всего показанием к СРЛ явились абсцесс сальниковой сумки (3 случая), гнойное расплавление забрюшинной клетчатки (3 случая), аррозионное кровотечение (2 случая). Во всех этих случаях предпринято вмешательство через окно в брюшной стенки, то есть через оментобуростомию.
При продолжающейся деструкции головки поджелудочной железы (3 случая) в 3-х случаях производилась ревизия ретроперитонеальных образований. При этом использован прием Кохера — мобилизация двенадцатиперстной кишки (ДПК) вместе с головкой поджелудочной железы путем рассечения тонкого заднего листка париетальной брюшины (несколько латеральнее ДПК) и постепенного отведения указанного блока в медиальном направлении (рис.1).
Рассекают брюшину и постепенно мобилизуют подлежащие органы в медиальном направлении, включая левую половину толстой кишки, селезенку и хвост поджелудочной железы. Как рекомендуют хирурги, имеющие большой опыт СРЛ, у больных с панкреонекрозом, необходимо ликвидировать застой желчи, как важный патогенетический механизм развития деструктивного процесса в поджелудочной железе (рис.2.). Рекомендуется удалить желчный пузырь и дренировать холедох через пузырный проток.
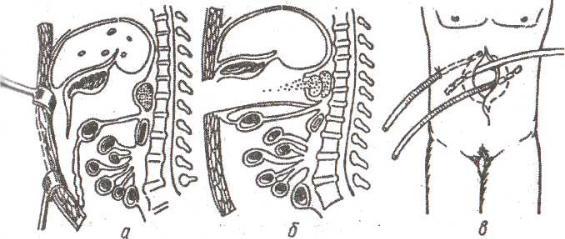
Рис. 1. Ревизия (а), санация (б) и дренирование (в) сальниковой полости

Рис. 2. Дренирование брюшной полости и холедоха при панкреатогенном перитоните
Хирурги, имеющие опыт ургентной хирургии поджелудочной железы рекомендуют при ООП уже при первичной лапаротомии произвести париетальную деперитонизацию и абдоминизацию поджелудочной железы с последующей регулярной, активной хирургической санацией через оментобурзостомы.
Такая технология является основным саногенным фактором, способствующим самоограничению, а затем и ликвидации гнойно-некротического процесса. В целом, указанная технология дренирования и санации может быть принята на вооружение как метод выбора и как базовый метод при СРЛ.
Таким образом в заключении можно констатировать, что процесс нормализации послеоперационного общего состояния больных напрямую зависит от наличия у них ПОН. Более быстрое восстановление происходит у больных, не имеющих ПОН. Послеоперационная летальность у оперированных больных наблюдалась лишь у тех, кто имел ПОН. Летальность в группах сравнения наблюдалась лишь у больных с ПОН. Летальность в подгруппе Б превышает летальность в аналогичной подгруппе больных на 33,3 %;
Значение ПКХ для благоприятного исхода патологии не высокое. Между тем, для неблагоприятного исхода значение ПОН имеет большое значение. Нужно отметить, что все осложнения в послеоперационном периоде носили поздний характер.
У больных шансы на неблагополучный исход в 2,6 раза превышает таковую благоприятного исхода. Практически, исход не зависит от ПКХ, а целиком зависит от степени выраженности ПОН.
Литература:
- Борисов А. Е., Федоров А. В., Земляной В. П. Ошибки, осложнения и летальность у больных с острыми хирургическими заболеваниями органов брюшной полости. — Санкт-Петербург: ЭФА, 2000. — 162 с.
- Бояринцев Н. И., Николаев Е. В., Ташкинов Н. В. и др. Повторные операции в экстренной и плановой абдоминальной хирургии // Дальневосточный медицинский журнал. — 2005. — № 1. — С.18–21..
- Глабай В. П., Шаров А. И., Абрамов А. А. Релапаротомии после неотложных операций на органах брюшной полости // Медицинский академический журнал. — 2003. — Том 3, № 2. — С.28–29.
- Иманов Б. М. Оптимизация и оценка эффективности тактико-технических решений при остром деструктивном панкреатите // Автореф. дис. … канд. мед. наук. 14.00.27. — Бишкек, 1999. — 20 с.
- Сопуев А. А., Иманов Б. М. Хирургическое лечение острого деструктивного панкреатита (Методические рекомендации): Утв. УМС МЗ КР. — Бишкек, 1998. — 17 с.







