Проведено ранжирование силы окислителей пероксида водорода, озона и синглетного кислорода по критерию глубины окисленности разных марок технического углерода. Предложено для использования в практике сочетание H₂O₂ с синглетным кислородом.
Ключевые слова: технический углерод, окисление, функциональные группы, пероксид водорода, озон, синглетный кислород.
Технический углерод — продукт глубокой переработки углеводородов в условиях высокотемпературного термоокислительного пиролиза. Он представляет собой дисперсные частицы глобулярного строения, объединённые в прочные сростки — агрегаты. Глобулы технического углерода состоят из пачек графенов, располагающихся с уменьшающейся плотностью их упаковки к центру глобулы. В ходе получения технического графеновые слои, находящиеся на поверхности глобул, подвергаются частичной газификации в среде отходящих газов СО2, СО, Н2О, при этом краевые углеродные атомы насыщаются кислородом в виде функциональных групп [1]. В соответствии с термодинамической устойчивостью на поверхности технического углерода превалируют группы хинонного типа [1,2]. Для ряда практических задач наибольший интерес представляют протоногенные группы, такие как карбоксильные и фенольные. Однако, они являются термодинамически не устойчивыми в условиях синтеза технического углерода. Их синтез проводят в постреакторных условиях при низких температурах, получая функционализированный технический углерод.
Окисление технического углерода необходимо для повышения его взаимодействия с компонентами композиционных материалов, улучшения смачивания поверхности и придания функциональных свойств композитам. Известно, что степень окисленности технического углерода нарастает при его окислении в три стадии. На первой стадии из хроменовых групп образуются гидроксильные и фенольные. На второй стадии фенольные группы окисляются в карбоновые или хинонные. На третьей стадии окисления на поверхности технического углерода образуются группы, содержащие 2 атома кислорода. Они сильно снижают рН водной суспензии и увеличивают полярность поверхности технического углерода. Степень окисленности технического углерода условно характеризуют по соотношению концентраций карбоксильных групп на его поверхности к фенольным. Для определения концентрации функциональных групп в процессе окисления технического углерода используют титриметрический метод их селективной нейтрализации основаниями разной силы — известный как метод Boehm H. P. [3,4].
Из большого ряда окислителей — кислот, солей и газов — рациональными являются такие, которые не загрязняют технический углерод и отходящие газы его производства. Наиболее перспективными являются перекись водорода, озон, кислород и их смеси. Все они относятся к активным формам кислорода (АФК).
Непосредственное влияние вариантов окислителей группы АФК на формирование функционального состава поверхности технического углерода в научной литературе практически не освещено. В патентной литературе с целью снижения показателя рН водной суспензии ТУ на 3–5 ед. от первоначального использовали как жидкофазное окисление технического углерода пероксидом водорода [5–7], так и газофазное окисление озоном [8–10] или смесью кислородсодержащего газа с парами пероксида водорода [11].
Патентная активность к процессам окисления технического углерода обусловлена всё более возрастающей потребностью в функционализированном техническом углероде. Однако, малая изученность взаимодействия технического углерода с АФК не позволяет выявить оптимальные технологические приёмы окисления технического углерода АФК для селективного накопления функциональных групп заданного строения и регулировать его степень окисленности. Не изучено также влияние свойств технического углерода на результат окисления разными АФК.
Целью данного исследования является сравнение окислительной способности пероксида водорода, озона и синглетного кислорода по отношению к техническому углероду разных марок.
Объектами исследования служили три марки технического углерода, отличающиеся размерами глобул и степенью их газификации, соответствующей коэффициенту шероховатости их поверхности (таблица 1). Образцы N 326 и N121 получены на предприятии ОАО «Омсктехуглерод», П366-Э — в ИППУ СО РАН.
Кш оценивали по отношению полной удельной поверхности методом БЭТ к внешней по статистической толщине слоя азота, определяемых по методике АSTM D6556.
Таблица 1
Физико-химические свойства образцов технического углерода
|
Показатели |
Значения показателей |
||
|
N326 |
N121 |
П366-Э |
|
|
Средний диаметр глобул, нм |
27 |
19 |
32 |
|
Удельная поверхность по адсорбции азота (метод БЭТ АSTM D6556), м2/г |
77 |
118 |
173 |
|
Коэффициент шероховатости поверхности, Кш, отн.ед |
1,0 |
1,1 |
1,6 |
Из данных в таблице 1 следует, что поверхность технического углерода П366-Э является более шероховатой, что является следствием его термоокислительной обработки при получении. Большая шероховатость поверхности способствует увеличению скорости разложения пероксида водорода.
Окисление образцов проводили в движущемся слое гранул при температуре 20°С в атмосфере воздуха в течение 5 мин. Раствор перекиси водорода распыляли на гранулы (1:1 по массе). Воздух, обогащенный озоном, получали из бытового озонатора O3ONER (Россия, «Формула здоровья») с производительностью по озону 400 мг/ч (~ 0,005 % масс.), воздух,обогащенный синглетным кислородом, — с помощью устройства AIRNERGY+ Basis Plus (Германия, «Airnergy AG») с фотокаталитическим активированием (λ 634 нм) и скоростью потока 4 л/ч (~ 0,0005 % масс.).
Окислители по-разному влияют на состав и содержание кислотных функциональных групп на поверхности технического углерода (рис.1).
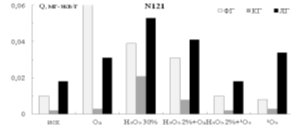
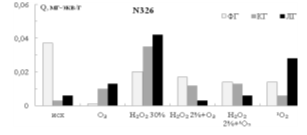
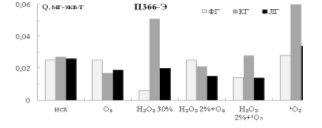
Рис. 1. Влияние окислительных систем на содержание кислотных функциональных групп разных марок технического углерода
По увеличению содержания карбоксильных групп наиболее глубоко идёт окисление 30 %-ным раствором перекиси водорода Н2О2. Озон и его комбинации с 2 %-ным раствором Н2О2 для технического углерода менее эффективны. Из сравнения окислительной способности озона и синглетного кислорода в отношении технического углерода второй реагент действует сильнее.
Важно отметить, что использование синглетного кислорода при окислении технического углерода в газовой фазе приводит к образованию лактоновых групп, тогда как при использовании в качестве окислителя синглетного кислорода в сочетании с 2 %-ным раствором перекиси водорода наблюдается преимущественное образование фенольных и карбоксильных групп — предшественников лактоновых групп.
На рис. 2 показано, что технический углерод марки N121 эффективнее окисляется при использовании газовой фазы ¹O₂ и системы (2 % H₂O₂ + ¹O₂) по сравнению с 30 % H₂O₂.
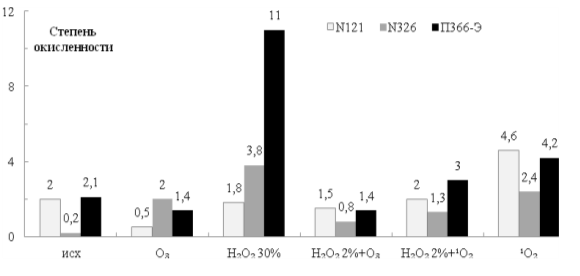
Рис. 2. Влияние состава АФК на степень окисленности разных марок технического углерода
Все использованные окислители (за исключением O3) повышают степень окисленности технического углерода марки П366-Э, и по снижению эффективности располагаются в ряд
30 % H₂O₂ > ¹O₂ > (2 % H₂O₂ + ¹O₂) > (2 % H₂O₂ +O₃), O₃.
Таким образом, наибольшим окислительным действием на технический углерод обладает 30 % раствор пероксида водорода.
Однако его использование в производстве технического углерода затруднено из-за бурного разложения пероксида водорода с выделением кислорода и, соответственно, роста давления в аппарате — смесителе-грануляторе, деструкции сформировавшихся гранул.
Более эффективно окисление технического углерода «сухим» способом воздухом, активированным синглетным кислородом, либо «мокрым» способом, смачивая его поверхность 2 %-ным раствором пероксида водорода в атмосфере воздуха, активированного синглетным кислородом.
Литература:
- Раздьяконова Г. И. Получение и свойства дисперсного углерода: монография. Омск: Изд-во ОмГТУ, 2014.-236 с.
- LiN., MaX., ZhaQ., KimK., ChenY., SongCh. Maximizing the number of oxygen-containing functional groups on activated carbon byusing ammonium persulfate and improving the temperature-programmed desorption characterization of carbon surface chemistry Carbon 49.15 (2011) 5002–5013
- Boehm H. P. Some aspects of the surface chemistry of carbon blacks and other carbons. Carbon 1994. V. 32 (5). P. 759–69.
- Boehm H. P. Surface oxides on carbon and their analysis: A critical assessment. Carbon 2002. V. 40. P. 145–149.
- Patent 3717494 US. Process for the production of color black by the furnace process./ Jager G., Kuhner G.– Fil. 28.05.1970.
- Patent 48793354 US. Carbon black pigments./Fumio Hirota, Tsutomu Kado, Shosuke Oku, Noboru Watanabe.– Fil. 22.09.1987.
- Patent 6120594 US. Hydrogen peroxide oxidation of carbon black / J. C. Curtis,.A. Joyce, R. L. Taylor.– Fil. 28.04.1999; iss. 19.09.2000.
- Patent 6471933 US. Ozone-oxidized carbon black composition with low conductivity and improved color./ Dotson. A.O.– Fil. 26.02.1997.
- Patent 3216843 US. Treatment of carbon black./ Heller G. L., Mcree N. N.– Fil. 21.12.1962.
- Patent 3245820 US. Preparation of long-flow carbon black./ Eckert F. J., Melore P. J.– Fil. 07.02.1963
- Patent 3279935 US. Oxidation of carbon black./ Daniell A. E., Peterson W. R.– Fil. 11.06.1963.







